题目内容
12.如表各组溶液电解一段时间后,再加入相关物质,溶液能恢复原来组成的是( )| 电解质溶液 | 阳极 | 阴极 | 加入的物质 | |
| A | NaCl溶液 | 碳 | 铁 | 盐酸 |
| B | 稀硫酸 | 铜 | 碳 | 水 |
| C | 硫酸铜溶液 | 铜 | 碳 | 硫酸铜 |
| D | NaOH溶液 | 碳 | 铁 | 水 |
| A. | A | B. | B | C. | C | D. | D |
分析 电解质在通电一段时间,加入物质能使溶液恢复到电解前的状态,说明依据电解原理分析电解了什么物质,要想让电解质复原,就要加入溶液中减少的物质,即:出什么加什么即可.
解答 解:A、以Fe和C为电极,电解氯化钠,阳极氯离子放电,阴极氢离子放电,通电一段时间后放出氯气和氢气,电解质复原,应该通入HCl,故A错误;
B、以Cu为阳极,电解硫酸,阳极Cu失电子,阴极上是氢离子得电子生成氢气,加入水,电解质不会复原,故B错误;
C、以Cu为阳极,电解硫酸铜,阳极铜本身失电子,阴极铜离子得电子,通电一段时间后电解质溶度和组成都不变,不许加入任何物质,故C错误;
D、以C为阳极,电解NaOH溶液,阳极氢氧根离子放电,阴极氢离子放电,相当于电解水,通电一段时间后仍为氢氧化钠溶液,可以加水让溶液复原,故D正确.
故选D.
点评 本题考查学生电解原理的知识,理解电解过程的物质变化和被电解的物质是解题关键,可以根据所学知识来回答,难度中等.

练习册系列答案
相关题目
2.现有三组溶液:①汽油和氯化钠溶液 ②49%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸发、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
7.下列说法不正确的是( )
| A. | 用10mL量筒量取6.8mL稀H2SO4 | |
| B. | 用碱式滴定管量取15.80mLKMnO4溶液 | |
| C. | 酸碱中和滴定时,滴定管需用标准液或待测液润洗 | |
| D. | 中和热测定时,氢氧化钠溶液稍过量的目的是为了保证盐酸完全被中和 |
4.下列叙述不正确的是( )
| A. | 标准状况下,22.4LNO与11.2LO2混合,混合气体所含分子数为NA | |
| B. | 1molAl3+含有的核外电子数为10NA | |
| C. | 常温常压下,1mol氮气含有的原子总数为NA | |
| D. | 1L1mol/LFeCl3溶液全部制成胶体,其中含胶粒的数目小于NA |
1.25℃时,下列各组离子在指定溶液中可能大量共存的是( )
| A. | 无色溶液中:NH4+、Cu2+、CO32-、Cl- | |
| B. | 中性溶液中可能大量存在Na+、Ba2+、Cl-、NO3- | |
| C. | pH值为1的溶液:Na+、Al3+、CH3COO-、SO42- | |
| D. | 由水电离的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、K+、HCO3-、Br- |
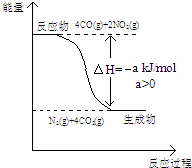 研究NOx、SO2、CO等大气污染气体的处理具有重要意义.
研究NOx、SO2、CO等大气污染气体的处理具有重要意义.