题目内容
 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是( )| A、铁是阳极,电极反应为Fe-2e-+2OH-═Fe(OH)2 |
| B、电解一段时间后,镍电极附近溶液的pH减小 |
| C、若离子交换膜为阴离子交换膜,则电解过程中氢氧根向阳极移动 |
| D、每制得1mol Na2FeO4,理论上可以产生67.2L气体 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4),铁失电子生成高铁酸钠,则铁作阳极,镍作阴极,阳极上铁失电子发生氧化反应,电极方程式为Fe-6e-+8OH-═FeO42-+4H2O,阴极发生还原反应,电极方程式为2H++2e-=H2↑,结合电极方程式解答该题.
解答:
解:A.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4),铁失电子生成高铁酸钠,则铁作阳极,镍作阴极,电极反应式为Fe+8OH--6e-=FeO42-+4H2O,故A错误;
B.镍电极上氢离子放电生成氢气,电极方程式为2H++2e-=H2↑,氢离子浓度减小,所以溶液的pH增大,胡B错误;
C.阴离子交换膜只允许阴离子通过,阴离子移向阳极,应从左向右移动,故C正确;
D.温度和压强未知,所以无法计算生成气体体积,故D错误.
故选C.
B.镍电极上氢离子放电生成氢气,电极方程式为2H++2e-=H2↑,氢离子浓度减小,所以溶液的pH增大,胡B错误;
C.阴离子交换膜只允许阴离子通过,阴离子移向阳极,应从左向右移动,故C正确;
D.温度和压强未知,所以无法计算生成气体体积,故D错误.
故选C.
点评:本题考查了电解原理,正确判断阴阳极及发生的反应是解本题关键,易错选项是D,注意气体摩尔体积的适用范围和条件,为易错点.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
化学与人类生活、环境保护、能源开发、资源利用等密切相关.下列说法不正确的是( )
| A、在食用盐中添加适量的碘酸钾 |
| B、用聚氯乙烯塑料袋包装食品 |
| C、在食品加工中科学使用食品添加剂 |
| D、研发高效低毒的农药,降低蔬菜的农药残留量 |
以H2、O2、熔融盐Na2CO3组成的燃料电池来电解制备N2O5,装置如图所示,其中Y为CO2.下列说法错误的是
( )
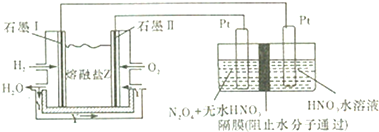
( )

| A、石墨Ⅱ电极上发生反应的电极反应式为:O2+4e-+2CO2═2CO32- |
| B、在电解池中生成N2O5的电极反应式为:N2O4+2NO3--2e-═2N2O5 |
| C、放电时熔融盐中CO32-向石墨I电极方向移动 |
| D、每消耗11.2L氢气,理论上可以制得108g N2O5 |
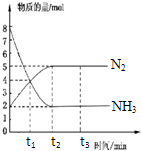 在体积一定的密闭容器中发生反应:2NH3(g)?N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)随时间变化的关系如图所示.下列叙述正确的是( )
在体积一定的密闭容器中发生反应:2NH3(g)?N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)随时间变化的关系如图所示.下列叙述正确的是( )| A、t1时反应达到平衡 |
| B、t3时,v正(N2)>v逆(N2) |
| C、t2时和t3时n(H2)相等 |
| D、t3后,若体积不变充He,反应速率增大 |
下列离子或分子组能大量共存,且满足相应要求的是( )
| A、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 |
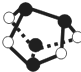 NA表示阿伏加德罗常数的值,下列说法正确的是( )
NA表示阿伏加德罗常数的值,下列说法正确的是( )| A、0.5mol雄黄(As4S4结构如图)含有NA个S-S键 | ||||
| B、7.8g Na2S和7.8g Na2O2中含有的阴离子数目均为0.1NA | ||||
C、1.8g
| ||||
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
下列实验操作或装置符合实验要求的是( )


| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、84g NaHCO3晶体中含有NA个CO32- |
| B、0.1mol?L-1K2CO3溶液中,阴离子总数大于0.1NA |
| C、1.8g石墨和C60的混合物中,碳原子数目为0.15NA |
| D、标准状况下,22.4L CCl4中含有的共用电子对数目为4NA |