题目内容
5.下列说法正确的是( )| A. | 1mol任何物质都约含有6.02×1023个原子 | |
| B. | 物质的量为2mol的BaCl2中,含有Cl-个数为2NA | |
| C. | O2的摩尔质量是32 | |
| D. | 摩尔是物质的量的单位 |
分析 A.物质可能由原子、分子构成,且可能为多原子分子;
B.结合N=nNA及分子构成计算;
C.摩尔质量的单位为g/mol;
D.物质的量为基本物理量之一,其单位为摩尔.
解答 解:A.1mol由单原子构成的物质都约含有6.02×1023个原子,故A错误;
B.物质的量为2mol的BaCl2中,含有Cl-个数为4NA,故B错误;
C.O2的摩尔质量是32g/mol,故C错误;
D.物质的量为基本物理量之一,摩尔是物质的量的单位,故D正确;
故选D.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、物质的量、微粒数的关系为解答关键,侧重分析与应用能力的考查,注意选项A为易错点,题目难度不大.

练习册系列答案
相关题目
15.下列关于乙烯和乙烷的说法中,不正确的是( )
| A. | 乙烯属于不饱和链烃,乙烷属于饱和链烃 | |
| B. | 乙烯分子中所有原子处于同一平面上,乙烷分子中的原子不在同一平面上 | |
| C. | 乙烯分子中的 双键比乙烷分子中的 C-C 单键更稳定,性质更活泼 | |
| D. | 乙烯能使酸性 KMnO4 溶液褪色,乙烷不能 |
16.瑞典皇家科学院曾将诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家.下列分子中含有“手性碳原子”的是( )
| A. | CBr2F2 | B. | CH3CH(OH)COOH | C. | CH3CH2CH3 | D. | CH3CH2OH |
10.相同质量的下列有机物在氧气中充分燃烧,生成CO2最多的是( )
| A. | C4H10 | B. | C6H6 | C. | C6H14 | D. | C8H10 |
17.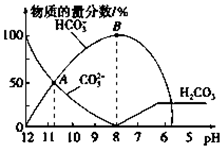 常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )
 常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )| A. | 在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-) | |
| B. | 当溶液的pH为7时,溶液的总体积大于20mL | |
| C. | 在B点所示的溶液中,浓度最大的离子是HCO3- | |
| D. | 在0.1 mol•L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
14.将2aL Al2(SO4)3和(NH4)2SO4的混合物溶液分为两等份,其中一份加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;另一份加入足量强碱并加热可得到c mol NH3气,则原混合溶液中的Al3+离子浓度(mol/L)为( )
| A. | $\frac{2b-c}{a}$ | B. | $\frac{2b-c}{2a}$ | C. | $\frac{2b-c}{3a}$ | D. | $\frac{2b-c}{6}$ |
15.五种主族元素在周期表中的位置如表所示.L的单质在常温常压下呈液态,且保存时需要用水液封.下列推断正确的是( )
| X | Y | Z | T | |
| L |
| A. | 原子半径:X<Y<Z<T<L | |
| B. | 气态氢化物的还原性:L>Z>T | |
| C. | 含x的两种盐溶液混合可能生成沉淀 | |
| D. | Y的含氧酸的酸性小于T的含氧酸 |
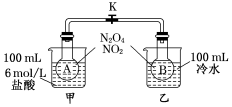 为测定温度对平衡的影响,设计了如下试验.
为测定温度对平衡的影响,设计了如下试验.