题目内容
下列叙述正确的是( )
| A、25℃时,MgCO3饱和溶液中c(Mg2+)=2.6×10-3mol?L-1,CaCO3饱和溶液中c(Ca2+)=5.3×10-5mol?L-1,向浓度均为0.1 mol?L-1的MgCl2和CaCl2混合溶液中逐滴加入0.1 mol?L-1的Na2CO3溶液,首先生成 CaCO3沉淀 |
| B、0.1 mol/LNa2CO3溶液和0.1 mol/L NaHSO4溶液等体积混合,溶液中c(Na+)+c(H+)=c(CO32-)+c(SO42-)+c(HCO3-)+c(OH-) |
| C、pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 |
| D、已知Fe3++2 I-=Fe2++I2,则浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 |
考点:难溶电解质的溶解平衡及沉淀转化的本质,酸碱混合时的定性判断及有关ph的计算,氯气的化学性质
专题:基本概念与基本理论
分析:A、溶度积小的物质先转化为沉淀;
B、依据溶液中阳离子所带的正电荷总数=阴离子所带的负电荷总数回答即可;
C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性;
D、据氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子分析.
B、依据溶液中阳离子所带的正电荷总数=阴离子所带的负电荷总数回答即可;
C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性;
D、据氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子分析.
解答:
解:A.25℃时,MgCO3饱和溶液中c(Mg2+)=2.6×10-3mol?L-1,CaCO3饱和溶液中c(Ca2+)=5.3×10-5mol?L-1,则Ksp(MgCO3)=6.76×10-6>Ksp(CaCO3)=2.8×10-9,所以向浓度均为0.1 mol?L-1的MgCl2和CaCl2混合溶液中逐滴加入0.1 mol?L-1的Na2CO3溶液,首先生成CaCO3沉淀,故A正确;
B、溶液中存在电中性原则,即:阳离子所带的正电荷总数=阴离子所带的负电荷总数,故c(Na+)+c(H+)=2c(CO32-)+2c(SO42-)+c(HCO3-)+c(OH-),故B错误;
C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性,故C错误;
D、氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子,氧化铁离子不是置换反应,故D错误,故选A.
B、溶液中存在电中性原则,即:阳离子所带的正电荷总数=阴离子所带的负电荷总数,故c(Na+)+c(H+)=2c(CO32-)+2c(SO42-)+c(HCO3-)+c(OH-),故B错误;
C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性,故C错误;
D、氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子,氧化铁离子不是置换反应,故D错误,故选A.
点评:本题主要考查的是难溶物的沉淀转化、溶液电中性原则、酸碱混合后pH值大小的判断、氧化性强弱比较,综合性较强,注意掌握.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
下列物质与其用途相符合的是( )
①ClO2-消毒剂
②NaHCO3-治疗胃酸过多
③明矾-做干燥剂
④硅-做光导纤维
⑤Na2O2-呼吸面具的供氧剂
⑥NaClO-漂白纺织物.
①ClO2-消毒剂
②NaHCO3-治疗胃酸过多
③明矾-做干燥剂
④硅-做光导纤维
⑤Na2O2-呼吸面具的供氧剂
⑥NaClO-漂白纺织物.
| A、②④⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、全部 |
类比推断法是研究物质性质的常用方法之一,可预测许多物质的性质.但类比推断法是相对的,不能违背客观实际.下列说法正确的是( )
| A、由溶解性CaCO3<Ca(HCO3)2,则溶解性Na2CO3<NaHCO3 |
| B、向Ca(ClO)2溶液中通入少量CO2可得到CaCO3,则向Ca(ClO)2溶液中通入少量SO2可得到CaSO3 |
| C、由O2与Li加热生成Li2O,则O2与Na加热生成Na2O |
| D、有Fe与S加热生成FeS,则Cu与S加热生成Cu2S |
下列反应中硫酸既表现氧化性,又表现酸性的有( )
A、2H2SO4(浓)+Cu
| ||||
B、2H2SO4 (浓)+C
| ||||
C、H2SO4 (浓)+NaCl
| ||||
| D、H2SO4+Na2SO3═Na2SO4+H2O+SO2↑ |
 磷单质及其化合物在工业有广泛应用.
磷单质及其化合物在工业有广泛应用.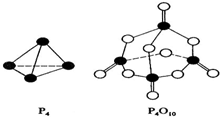

 利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是( )
利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是( )