题目内容
1.在25℃下,将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显中性(填“酸”“碱”或“中”);用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$.分析 在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$.
解答 解:在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{+})}{c(N{H}_{3}.{H}_{2}O)}$=$\frac{1{0}^{-7}×5×1{0}^{-3}}{0.5a-5×1{0}^{-3}}$=$\frac{1{0}^{-9}}{a-0.01}$;
故答案为:中;$\frac{1{0}^{-9}}{a-0.01}$.
点评 本题考查弱电解质电离,题目难度中等,根据电荷守恒确定溶液酸碱性,结合一水合氨电离平衡常数解答问题,注意二者混合后溶液体积增大一倍,物质浓度降为原来一半,为易错点.

练习册系列答案
相关题目
11.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s),△H=-216kJ•mol-1,反应物总能量小于生成物总能量 | |
| B. | 相同条件下,如果1 mol氢原子所具有的能量为E1,1mol氢分子的能量为E2,则2E1>E2 | |
| C. | 101kPa时,2H2(g)+O2(g)=2H2O(1),△H=-571.6kJ•mol-1,若生成气态水,△H小于-571.6kJ•mol-1 | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
12.串联电路中四个电解池分别装有0.5mol•L-1的下列溶液,用惰性电极电解,连接直流电源一段时间后,溶液pH最大的是( )
| A. | KNO3溶液 | B. | NaCl溶液 | C. | AgNO3溶液 | D. | CuCl2溶液 |
9.有以下四种物质:①标况下11.2LCO2 ②1g H2③1.204×1024个N2④4℃时18mlH2O,下列说法不正确的是( )
| A. | 分子个数:③>④>①=② | B. | 原子个数:③>④>①>② | ||
| C. | 质 量:③>①>④>② | D. | 体 积:③>④>①=② |
16.下列叙述正确的是( )
①其它条件不变时,缩小容器体积,平衡H2(g)+I2(g)?2HI(g)不移动,体系颜色不变
②常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液中:Na+、Al3+、SO42-、NO3-可大量共存
③将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
④为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸.
①其它条件不变时,缩小容器体积,平衡H2(g)+I2(g)?2HI(g)不移动,体系颜色不变
②常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液中:Na+、Al3+、SO42-、NO3-可大量共存
③将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
④为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸.
| A. | 全错 | B. | 只有④正确 | C. | ①③④正确 | D. | ①②③正确 |
6.如图为用球棍模型表示的某有机反应过程的示意图,该反应的类型是( )
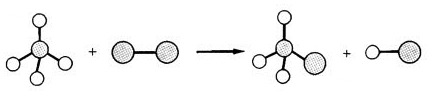

| A. | 取代反应 | B. | 加成反应 | C. | 聚合反应 | D. | 氧化反应 |
4.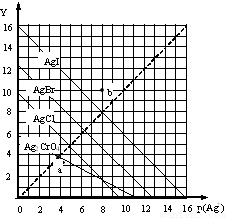 卤化银AgX的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标Y=-lgc(X-).下列说法正确的是( )
卤化银AgX的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标Y=-lgc(X-).下列说法正确的是( )
 卤化银AgX的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标Y=-lgc(X-).下列说法正确的是( )
卤化银AgX的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标Y=-lgc(X-).下列说法正确的是( )| A. | 该温度下AgCl的Ksp约为1×10-15 | |
| B. | a点时c(Ag+)=c(I-),AgI处于平衡状态 | |
| C. | b点可表示AgBr的不饱和溶液 | |
| D. | 该温度下AgCl、AgBr饱和溶液中:c(Cl-)<c(Br-) |