题目内容
10.下列说法正确的是( )| A. | 如果某化合物只含共价键,则其一定是共价化合物 | |
| B. | H2O2是由极性共价键和非极性共价键构成的非极性分子 | |
| C. | 两种酸溶液充分反应后的体系不可能为中性 | |
| D. | 碳、氮形成的氢化物常温下都是气态 |
分析 A.只含有共价键的化合物是共价化合物;
B.结构对称正负电荷中心重叠的分子属于非极性分子;
C.氧化还原反应的发生有可能使得溶液的酸碱性发生变化;
D.分子量较大的烃常温下为液体.
解答 解:A.只含有共价键的化合物是共价化合物,所以如果某化合物只含共价键,则其一定是共价化合物,故A正确;
B.H2O2是由极性共价键和非极性共价键构成,分子结构不对称,正负电荷中心不重叠,属于极性分子,故B错误;
C.反应2H2S+H2SO3=3H2O+S↓可以知道:氢硫酸和亚硫酸溶液充分反应后的溶液体系为中性,所以两种酸溶液充分反应后的体系可能为中性,故C错误;
D.分子量较大的烃常温下为液体,如辛烷常温下为液体,所以碳、氮形成的氢化物常温下不一定是气态,故D错误.
故选A.
点评 本题考查了共价键和共价化合物、分子极性的判断、氧化还原反应、烃的物理性质,题目难度不大,侧重于基础知识的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.有主族元素A、B、C、D、E,相对位置如图所示.C的原子序数是D的两倍.
(1)E位于元素周期表中第四周期,第VA族,该周期共有18种元素
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是(写酸的化学式)H2SO4
(3)上述五种元素的氢化物稳定性最强的是(写氢化物的化学式)H2O,用电子式表示该物质的形成过程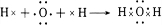 .
.
| D | ||
| A | B | C |
| E |
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是(写酸的化学式)H2SO4
(3)上述五种元素的氢化物稳定性最强的是(写氢化物的化学式)H2O,用电子式表示该物质的形成过程
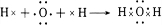 .
.
18.甲、乙两种非金属元素,能说明甲比乙的非金属性强的是( )
①甲单质比乙单质容易与氢气化合
②甲元素的单质能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强
④与某金属反应时,甲比乙得电子数多
⑤甲的单质熔沸点比乙的单质低.
①甲单质比乙单质容易与氢气化合
②甲元素的单质能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强
④与某金属反应时,甲比乙得电子数多
⑤甲的单质熔沸点比乙的单质低.
| A. | 只有③④ | B. | 只有①②⑤ | C. | 只有①②③ | D. | ①②③④⑤ |
5.关于如图所示装置的叙述,正确的是( )
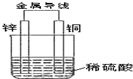

| A. | 铜片上没有气泡产生 | B. | 铜片质量逐渐减少 | ||
| C. | 电流从锌片经导线流向铜 | D. | 氢离子在铜片表面被还原 |
15.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. | 2-乙基丁烷 | B. | 二溴乙烷 | C. | 2-甲基丁烯 | D. | 苯甲醇 |
20.下列有关胶体的说法错误的是( )
| A. | 胶粒可以透过滤纸,不能透过半透膜 | |
| B. | 采用喷雾型药剂形成一定大小的液珠,可有效提高药物疗效 | |
| C. | 冶金工业的矿粒除尘利用了丁达尔效应 | |
| D. | 空气中的雾压现象体现了胶体的存在 |
 对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到:
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到: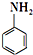 +H2SO4$\stackrel{170-180℃}{→}$
+H2SO4$\stackrel{170-180℃}{→}$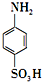 +H2O
+H2O