题目内容
下列有关各装置图及对应实验的描述正确的是( )
A、 电解精炼铝 |
B、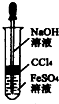 制备Fe(OH)2 |
C、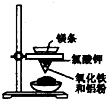 制得金属铁 |
D、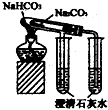 验证NaHC03和Na2C03的热稳定性 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氯化铝溶液中阴极氢离子放电;
B.四氯化碳的密度比水溶液的大,不能隔绝空气;
C.点燃镁条引发反应,铝热反应放出大量的热,可冶炼高熔点金属;
D.碳酸氢钠不稳定,受热易分解.
B.四氯化碳的密度比水溶液的大,不能隔绝空气;
C.点燃镁条引发反应,铝热反应放出大量的热,可冶炼高熔点金属;
D.碳酸氢钠不稳定,受热易分解.
解答:
解:A.氯化铝溶液中阴极氢离子放电,则电解精炼铝不能在溶液中进行,故A错误;
B.四氯化碳的密度比水溶液的大,不能隔绝空气,应将四氯化碳改为苯,故B错误;
C.点燃镁条引发反应,铝热反应放出大量的热,可冶炼高熔点金属,图中铝热反应实验合理,故C正确;
D.碳酸氢钠不稳定,受热易分解,则应在小试管中加入碳酸氢钠,可更好的体现对比性,故D错误;
故选C.
B.四氯化碳的密度比水溶液的大,不能隔绝空气,应将四氯化碳改为苯,故B错误;
C.点燃镁条引发反应,铝热反应放出大量的热,可冶炼高熔点金属,图中铝热反应实验合理,故C正确;
D.碳酸氢钠不稳定,受热易分解,则应在小试管中加入碳酸氢钠,可更好的体现对比性,故D错误;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及电解原理、物质的制备、铝热反应、稳定性比较等,把握物质的性质及实验原理为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
由两种气态烃组成的混合气体,其所含碳元素和氢元素的质量之比为24:3,则混合气体的组成及其体积比可能是( )
| A、CH4和C3H4,体积比为1:1 |
| B、C2H2和C2H6,体积比为3:1 |
| C、C2H4和C2H6,体积比为2:1 |
| D、C2H2 和C2H4,体积比为2:3 |
如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( ) 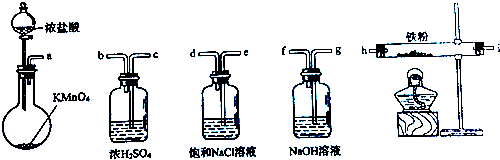

| A、a-b-c-d-e-e-f-g-h |
| B、a-e-d-c-b-h-i-g |
| C、a-d-e-c-b-h-i-g |
| D、a-c-b-d-e-h-i-f |
在一密闭容器中盛有V升Cl2和H2的混合气,在适宜条件下充分反应后再恢复到原状况时,气体体积仍为V升,将这些气体通过NaOH溶液时全部吸收,由此判断原混合气体中Cl2和H2的体积比可能是( )
| A、等于1:1 |
| B、小于1:1 |
| C、大于1:1 |
| D、小于或等于1:1 |
在反应5NH4NO3
2HNO3+4N2↑+9H2O中,发生氧化的氮原子与发生还原的氮原子的物质的量之比为( )
| ||
| A、3:5 | B、5:3 |
| C、5:8 | D、5:4 |
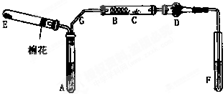 如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.