题目内容
8.已知: ,下列说法正确的是( )
,下列说法正确的是( )| A. | M能发生加聚反应、取代反应和氧化反应 | |
| B. | M的二氯代物有10种(不考虑立体异构) | |
| C. | N中所有碳原子在同一平面上 | |
| D. | 等物质的量的M、N分别完全燃烧,消耗O2的体积比为4:5 |
分析 A.M不含碳碳双键;
B.M结构对称,有2种H原子,结合位置异构判断;
C.N含有饱和碳原子,具有甲烷的结构特点;
D.M、N的分子式分别为C10H8、C10H18,结合分子式判断.
解答 解:A.M不含碳碳双键,不能发生加聚反应,故A错误;
B.M为萘,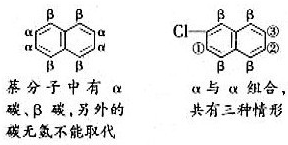
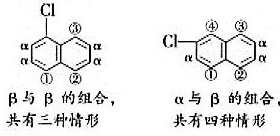 ,则萘的二氯取代物有10种,故B正确;
,则萘的二氯取代物有10种,故B正确;
C.N含有饱和碳原子,具有甲烷的结构特点,则所有的碳原子不可能都在同一个平面上,故C错误;
D.M、N的分子式分别为C10H8、C10H18,耗氧量分别为(10+$\frac{8}{4}$)、(10+$\frac{18}{4}$),二者比值为12:14.5,故D错误.
故选B.
点评 本题考查有机物的结构性质,为高频考点,侧重考查学生的分析能力,把握官能团与性质的关系为解答的关键,选项B解答的易错点,注意同分异构体的判断,题目难度中等.

练习册系列答案
相关题目
19.下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | Na2CO3•10H2O晶体久置后变成白色粉末 | Na2CO3•10H2O与空气中的CO2作用生成 NaHCO3 |
| B | 青铜(铜锡合金)在空气中久置表面会生成一层铜绿 | 发生电化学腐蚀,铜做负极 |
| C | 将过量SO2通入到KMnO4溶液中,溶液褪色 | SO2具有还原性,与 KMnO4发生氧化还原反应 |
| D | 向含有酚酞的 Na2CO3溶液中加入BaCl2固体, 溶液红色变浅 | Na2CO3溶液中的电离平衡发生移动 |
| A. | A | B. | B | C. | C | D. | D |
16.下列化学用语正确的是( )
| A. | Zn的电子排布式:1s22s22p63s23p64s2 | |
| B. | Fe2+的电子排布式:[Ar]3d6 | |
| C. | C的价电子轨道表示式: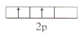 | |
| D. | HClO的电子式: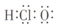 |
13.化学与生产、生活密切相关.下列与化学相关的说法正确的是( )
| A. | 水泥、水玻璃、水晶均属于硅酸盐产品 | |
| B. | 医用酒精和葡萄糖注射液可用丁达尔效应区分 | |
| C. | 氯水和食盐水消毒杀菌的原理相同 | |
| D. | 铵态氮肥和草木灰混合使用会降低肥效 |
20.下列关于有机化合物的说法不正确的是( )
| A. | 淀粉和纤纤维素互为同分异构体 | |
| B. | 油脂在碱性条件下的水解反应称为皂化反应 | |
| C. | 分子式为C5H10O2的有机物中能与NaHCO3溶液反应的有4种 | |
| D. | 在加热条件下,用新制的氢氧化铜悬浊液可鉴别乙醇和葡萄糖 |
17.实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )
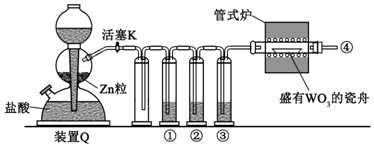

| A. | ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液 | |
| B. | 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度 | |
| C. | 结束反应时,先关闭活塞K,再停止加热 | |
| D. | 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 |
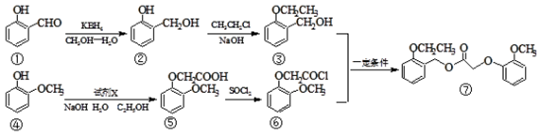
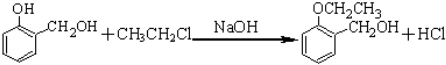 .
.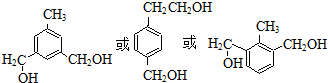 (写出一种
(写出一种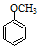 +HBr→
+HBr→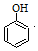 +CH3Br
+CH3Br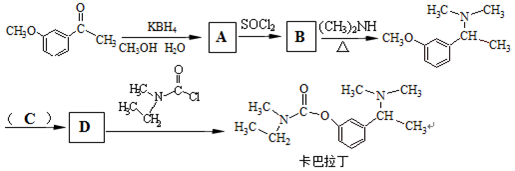
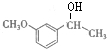 B:
B: C:HBrD:
C:HBrD: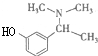 .
. .
.