题目内容
19.常温下,浓度均为0.1mol.L-1的6种溶液pH如下:| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
(1)常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是B>C>D>A(用A、B、C、D表示).
A.H2SiO3 B.H2SO3 C.H2CO3 D.HClO
(2)若要增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是NaHCO3或NaClO(填化学式).
(3)请写出上述NaClO溶液中通入少量CO2的化学方程式:NaClO+CO2+H2O=HClO+NaHCO3.
(4)等浓度的H2SO3和NaHSO3混合液,加入少量的强酸或强碱溶液,pH值都没有明显变化,请解其原因:加碱时发生反应:H2SO3+OH-=HSO3-+H2O;加酸时发生反应:HSO3-+H+=H2SO3(用离子方程式表示).
分析 (1)依据溶液Na2CO3,Na2SiO3,NaClO,Na2SO3的PH分析,亚硫酸是中强酸,同主族最高价含氧酸从上到下依次减弱;
(2)增大氯水中次氯酸浓度选择试剂和盐酸反应不能和次氯酸反应;
(3)NaClO溶液中通入少量CO2,生成碳酸氢钠和次氯酸;
(4)弱酸的电离程度和弱酸根的水解程度都很小,H2SO3和NaHSO3混合液能够形成缓冲溶液.
解答 解:(1)盐溶液的pH越大,盐的水解程度越大,盐的水解程度越大的盐对应酸的酸性越弱,由溶液Na2CO3,Na2SiO3,NaClO,Na2SO3的PH可知,酸性:B>C>D>A;
故答案为:B>C>D>A;
(2)Na2CO3、Na2SiO3、Na2SO3水解显碱性和盐酸反应也可以和次氯酸反应不能增大次氯酸浓度,加入NaClO和盐酸反应生成次氯酸,平衡正向进行,增大次氯酸浓度;加入NaHCO3,和盐酸反应促进平衡正向进行,增大次氯酸浓度;加入NaHSO3能被次氯酸氧化,次氯酸浓度减小;
故答案为:NaHCO3或NaClO;
(3)NaClO溶液中通入少量CO2,生成碳酸氢钠和次氯酸,其反应的化学方程式为:NaClO+CO2+H2O=HClO+NaHCO3;
故答案为:NaClO+CO2+H2O=HClO+NaHCO3;
(4)向H2SO3和NaHSO3混合液中加入少量强酸时,能够生成亚硫酸,加入少量强碱时,能够生成亚硫酸氢根离子,溶液的pH变化不大,
故答案为:加碱发生反应:H2SO3+OH-═HSO3-+H2O; 加酸发生反应:HSO3-+H+═H2SO3.
点评 本题考查了盐类水解的应用,溶液pH的大小和溶液酸碱性的分析判断依据,化学平衡的移动原理分析,注意次氯酸的弱酸性和盐溶液的酸碱性实质,题目难度中等.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
9.月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一.氦的该种核素为( )
| A. | ${\;}_{1}^{1}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{5}$He | D. | ${\;}_{2}^{1}$He |
7.以氨气代替氢气来研发氨燃料电池是当前科研的一个热点.氨燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O有关下列说法错误的是( )
| A. | 氨燃料电池在放电时,氨气被氧化 | |
| B. | 氨燃料电池在放电时,正极反应为:2NH3+6e-+6OH-=N2+6H2O | |
| C. | 以氨气代替氢气的主要原因是:氨气易液化易储存 | |
| D. | 氨燃料电池产物为无污染的氮气和水,属于环境友好电池 |
4.主链含5个碳原子,有甲基、乙基 2 个支链的烷烃有( )
| A. | 2 种 | B. | 3 种 | C. | 4 种 | D. | 5 种 |
11.某有机化合物D的结构为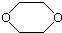 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得:
烃A$→_{①}^{Br_{2}}$B$→_{②}^{NaOH溶液}$C$→_{③}^{浓硫酸}$D,下列相关说法中正确的是( )
 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得:烃A$→_{①}^{Br_{2}}$B$→_{②}^{NaOH溶液}$C$→_{③}^{浓硫酸}$D,下列相关说法中正确的是( )
| A. | 烃A为CH3CH3 | B. | 反应②属于消去反应 | ||
| C. | 反应①②③都属于取代反应 | D. | 化合物D属于醚 |
8.在恒温恒容条件下,能使A(g)+2B(g)?C(g)+D (g) 正反应速率增大的措施是( )
| A. | 增大D的浓度 | B. | 减小C的浓度 | C. | 减小B的浓度 | D. | 减小压强 |
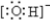 ,B转化为C的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
,B转化为C的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.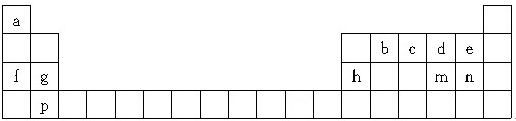
 ,其中含有的
,其中含有的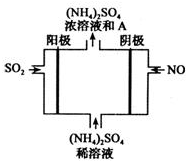 经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.
经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.