题目内容
17.t℃时,将2mol SO2和1mol O2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),2min时反应达到化学平衡,此时测得反应物O2还剩余0.2mol,请填写下列空白:(1)从反应开始到化学平衡,生成SO3的平均反应速率为0.4mol/(L•min);平衡时SO2转化率为80%.
(2)下列叙述能证明该反应已达到化学平衡状态的是ABE.
A.容器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2n mol SO2的同时消耗n mol O2
E.相同时间内消耗2n mol SO2的同时生成n mol O2
(3)t℃时,该反应的平衡常数为160
(4)t1℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了10%.SO2的转化率为40%.
分析 (1)2SO2(g)+O2(g)?2SO3(g),
开始(mol) 2 1 0
反应(mol) 1.6 0.8 1.6
平衡(mol) 0.4 0.2 1.6
v(SO3)=$\frac{\frac{△n}{V}}{△t}$;平衡时SO2转化率=$\frac{反应的二氧化硫物质的量}{反应初始二氧化硫物质的量}$×100%;
(2)化学平衡状态的标志:正反应速率等于逆反应速率,平衡混合物中各组成成分的含量不变,据此进行判断;
(3)建立平衡状态,根据平衡常数公式计算平衡常数;
(4)t2℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,设二者起始物质的量均为1mol,反应达到平衡时,混合气体体积减少了10%,则气体物质的量减小2mol×10%=0.2mol,利用差量法计算参加反应二氧化硫的物质的量,进而计算SO2的转化率.
解答 解:(1)2SO2(g)+O2(g)?2SO3(g),
开始(mol) 2 1 0
反应(mol) 1.6 0.8 1.6
平衡(mol) 0.4 0.2 1.6
v(SO3)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{1.6mol}{2L}}{2min}$=0.4mol/(L•min);平衡时SO2转化率=$\frac{反应的二氧化硫物质的量}{反应初始二氧化硫物质的量}$×100%=$\frac{1.6mol}{2mol}×100%$=80%,
故答案为:0.4mol/(L•min);80%;
(2)A.容器内压强不再发生变化,说明反应前后气体物质的量不变,正反应速率等于逆反应速率,反应达到平衡状态,故A正确;
B.SO2的体积分数不再发生变化,说明各物质的物质的量不变,正反应速率等于逆反应速率,反应已经达到平衡状态,故B正确;
C.容器内气体原子总数始终不变,无法判断是否达到平衡状态,故C错误;
D.相同时间内消耗2n mol SO2的同时消耗n mol O2,表示的都是正反应速率,无法判断正逆反应速率是否相等,故D错误;
E.相同时间内消耗2n mol SO2等效于消耗n mol O2,同时生成n mol O2,正反应速率等于逆反应速率,反应达到平衡状态,故E正确;
故答案为:ABE;
(3)此反应平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})×c({O}_{2})}$=$\frac{(\frac{1.6mol}{2L})^{2}}{(\frac{0.4mol}{2L})^{2}×(\frac{0.2mol}{2L})}$=160,故答案为:160;
(4)t2℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,设二者起始物质的量均为1mol,反应达到平衡时,混合气体体积减少了10%,则气体物质的量减小2mol×10%=0.2mol,
2SO2(g)+O2(g)?2SO3(g) 物质的量减小
2 1 2 1
0.4mol 0.4mol 0.2mol
故SO2的转化率=$\frac{0.4mol}{1mol}$×100%=40%,
故答案为:40%.
点评 本题考查化学平衡计算及化学平衡状态判断,为高频考点,侧重考查学生分析、判断及计算能力,注意:只有“反应前后改变的物理量”才能作为平衡状态的判断依据,难点是正确选取化学平衡状态的依据.

| A. | 5种 | B. | 7种 | C. | 9种 | D. | 11种 |
| A. | 氯化钠的电子式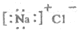 | B. | 次氯酸的电子式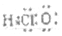 | ||
| C. | HCl分子的电子式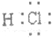 | D. | 氯原子的结构示意图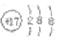 |
| A. | 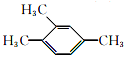 1,2,4-三甲苯 1,2,4-三甲苯 | B. |  2,2,4,4一四甲基戊烷 2,2,4,4一四甲基戊烷 | ||
| C. | 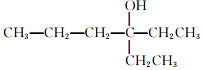 1,1-二乙基-1-丁醇 1,1-二乙基-1-丁醇 | D. |  1,3--溴丙烷 1,3--溴丙烷 |
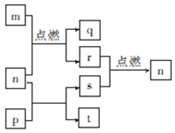 短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:Z>Y | |
| B. | 化合物p中只存在离子键 | |
| C. | 图示转化关系涉及的反应均为氧化还原反应 | |
| D. | 最简单气态氢化物的稳定性:W>X |
| 选项 | 实验目的 | 实验操作 |
| A | 称取2.0g NaOH固体 | 先在左、右两托盘上各放一张滤纸,然后在有盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 检验试液巾是否含有NH4+ | 取少量试液于试管巾,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| C | 除去CO2中混有的杂质SO2 | 将混合气体通入盛有澄清石灰水的洗气瓶中 |
| D | 验证金属钠比铜活泼 | 将钠加入1.0mol•L-1的CuSO4溶液中 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 2 | B. | 12 | C. | 26 | D. | 11 |
反应过程中测定的部分数据见表(反应过程中条件不变):
| t/s | 0 | 30 | 150 | 250 | 350 | 450 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x |
(1)x 的值是0.2;
(2)0-50s 内,用PCl3的浓度变化表示的化学反应速率是0.0016mol/(L•s);
(3)250s 以后,Cl2的物质的量不再改变的原因是250s达到平衡,正逆反应速率相等,条件不变,各组分的物质的量都不再变化;
(4)250s 时,容器中Cl2的物质的量是0.2mol,PCl5的物质的量是0.8mol,PCl5的转化率是20%.