题目内容
下列离子方程式与所述事实相符且正确的是( )
| A、用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
| B、用双氧水和稀硫酸可以雕刻印刷电路板:Cu+H2O2+2H+=Cu++2H2O |
| C、KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=2H2O+I2 |
| D、澄清石灰水与过量苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O. |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硫氰化钾是络合物不是沉淀;
B.二者反应生成铜离子,且电荷不守恒;
C.二者发生氧化还原反应生成碘和水;
D.二者反应生成碳酸钙、碳酸钠和水.
B.二者反应生成铜离子,且电荷不守恒;
C.二者发生氧化还原反应生成碘和水;
D.二者反应生成碳酸钙、碳酸钠和水.
解答:
解:A.硫氰化钾是络合物不是沉淀,离子方程式为Fe3++3SCN-=Fe(SCN)3,故A错误;
B.二者反应生成铜离子,且电荷不守恒,离子方程式为Cu+H2O2+2H+=Cu2++2H2O,故B错误;
C.二者发生氧化还原反应生成碘和水,离子方程式为2I-+H2O2+2H+=2H2O+I2,故C正确;
D.二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2OH-+2HCO3-=CaCO3↓+H2O+CO32-,故D错误;
故选C.
B.二者反应生成铜离子,且电荷不守恒,离子方程式为Cu+H2O2+2H+=Cu2++2H2O,故B错误;
C.二者发生氧化还原反应生成碘和水,离子方程式为2I-+H2O2+2H+=2H2O+I2,故C正确;
D.二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2OH-+2HCO3-=CaCO3↓+H2O+CO32-,故D错误;
故选C.
点评:本题考查离子方程式正误判断,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等,易错选项是D,要注意反应物的量,为易错点.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
1molMgSO4?7H2O含有结晶水的质量为( )
| A、16g | B、18g |
| C、112g | D、126g |
下列叙述正确的是( )
| A、氢氧化钠的摩尔质量是40g |
| B、1molNaOH的质量是40g/mol |
| C、1gH2和1gN2所含分子数相等 |
| D、阿伏伽德罗常数个钠原子的质量是23g |
下列离子方程式正确的是( )
| A、石灰水与过量碳酸氢钠溶液反应:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
| B、过量的CO2通入NaOH溶液中:CO2+OH-═HCO3- |
| C、硫酸铜与氢氧化钡溶液混合:Cu2++2OH-=Cu(OH)2 |
| D、氧化铜与稀硫酸反应:2H++O2-=H2O |
下列电离方程式正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、NaHSO4═Na++H++SO42- |
| C、CH3COOH═CH3COO-+H+ |
| D、Ba(OH)2═Ba2++OH- |
经测定,一瓶气体中只含有C、H两种元素,通常情况下这瓶气体不可能是( )
| A、一种化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物 |
| D、两种单质 |
在容积为672mL的烧瓶里充满NO、NO2的混合气体,将其倒立在水槽里,去塞后再通入280mL氧气,恰好完全反应,且水充满烧瓶(气体体积都已折合为标准状况),下列有关叙述中,正确的是( )
| A、总反应为NO+NO2+O2+H2O═2HNO3 |
| B、总反应为4NO+8NO2+5O2+6H2O═12HNO3 |
| C、生成硝酸的物质的量浓度接近0.03 mol/L |
| D、生成硝酸的物质的量浓度约为0.45 mol/L |
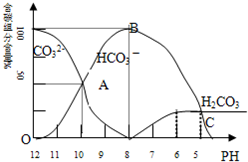 常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示.回答下列问题:
常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示.回答下列问题: