��Ŀ����
16��Na2SO3Ӧ�ù㷺�����ù�ҵ�ϼ�������Ҫ�ɷ�Na2CO3���������᳧β���е�SO2�Ʊ���ˮNa2SO3�ijɱ��ͣ��������ԣ����������£�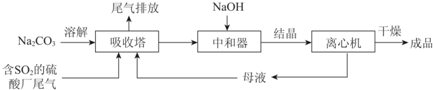
��1������˵����������ŷ�SO2���µĻ������⣺���꣮
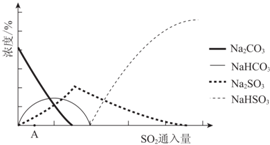
��2��ͼΪ��������Na2CO3��Һ��SO2��Ӧ��������Һ��ɱ仯������ڷ�Ӧ��ͼ��A����ǰ�������ӷ���ʽ��2CO32-+SO2+H2O=2HCO3-+SO32-��
��3���к����з�������Ҫ��Ӧ�Ļ�ѧ����ʽ��NaHSO3+NaOH=Na2SO3+H2O��
| ������ʾ�� ��Na2SO3��33��ʱ�ܽ������䱥����Һ������33������ʱ�������ܽ�Ƚ��ͻ�������ˮNa2SO3����ȴ��33������ʱ����Na2SO3•7H2O�� ����ˮNa2SO3�ڿ����в��ױ�������Na2SO3•7H2O�ڿ������ױ������� |
������Na2SO3���ܽ�ƽ�����NaOH������ԭ��Na2SO3�����ܽ�ƽ�⣺Na2SO3��s��
 2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ���
2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ����ڽᾧʱӦѡ�����Ѳ�����b��ѡ����ĸ����
a.95��100�����������ֱ������
b��ά��95��100������Ũ�����д�����������
c.95��100�����Ũ������ȴ�����½ᾧ
��5��Ϊ����Na2SO3��Ʒ���Ƿ�����Na2SO4����ѡ�õ��Լ���ϡ���ᡢBaCl2��Һ��
��6��KIO3�ζ����ɲⶨ��Ʒ��Na2SO3�ĺ����������½�0.1260g ��Ʒ����ˮ�����������ָʾ������������KIO3����Һ��x mol/L�����еζ�����Һǡ������ɫ��Ϊ��ɫ������KIO3����Һ���Ϊy mL��
�ٵζ��յ�ǰ��Ӧ�����ӷ���ʽ�ǣ�1IO3-+3SO32-=3SO42-+1I-��������ʽ����������
�ڳ�Ʒ��Na2SO3��M=126g/mol��������������3xy��100%��
���� ��1����������ᵼ�����ꣻ
��2����ͼ��֪�����ڷ�Ӧ��ͼ��A����ǰ��̼�������������Ӧ����̼���������������ƣ�
��3�����Ŷ�������ͨ����������������Ҫ�ǵõ����������ƣ��к�������Ҫ�ǽ�����������ת��Ϊ�����ƣ�ͬʱ̼�����Ʒ�Ӧ�õ�̼���ƣ�
��4����Na2SO3�ܽ����������ӣ�NaOH����ʹc��Na+����������Na2SO3�ܽ⣻
��������ȴ��33������ʱ����Na2SO3•7H2O��Ӧ�ڽϸ��¶�������Ũ�����д���������������������������
��5���������ȥ�������ƣ������Ȼ�����Һ������������ӣ�
��6����IO3-��SO32-����������ԭ��Ӧ�õ�SO42-��I-��IԪ�ػ��ϼ۽���6�ۣ�SԪ�ػ��ϼ�����2�ۣ����ϼ�������С������Ϊ6���ɵ�IO3-��ϵ��Ϊ1��SO32-��ϵ��Ϊ3���ٽ��ԭ���غ㡢����غ���ƽ��
�ڸ������ӷ���ʽ�����������Ƶ����ʵ�������������������������
��� �⣺��1����������ŷ�SO2�ᵼ�����귢����
�ʴ�Ϊ�����ꣻ
��2����ͼ��֪�����ڷ�Ӧ��ͼ��A����ǰ��̼�������������Ӧ����̼���������������ƣ���Ӧ���ӷ���ʽΪ��2CO32-+SO2+H2O=2HCO3-+SO32-��
�ʴ�Ϊ��2CO32-+SO2+H2O=2HCO3-+SO32-��
��3�����Ŷ�������ͨ����������������Ҫ�ǵõ����������ƣ��к�������Ҫ�ǽ�����������ת��Ϊ�����ƣ�ͬʱ̼�����Ʒ�Ӧ�õ�̼���ƣ���Ҫ��Ӧ��ѧ����ʽΪ��NaHSO3+NaOH=Na2SO3+H2O��
�ʴ�Ϊ��NaHSO3+NaOH=Na2SO3+H2O��
��4����Na2SO3�����ܽ�ƽ�⣺Na2SO3��s�� 2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ�������Na2SO3�ܽ⣬
2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ�������Na2SO3�ܽ⣬
�ʴ�Ϊ��Na2SO3�����ܽ�ƽ�⣺Na2SO3��s�� 2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ���
2Na+ ��aq��+SO32- ��aq����NaOH����ʹc��Na+����������ƽ�������ƶ���
��a����������ֱ�����ɣ�����ʹ���彦����������ʧ�ȣ���a����
b��ά��95��100������Ũ�����д��������������������������ɣ���b��ȷ��
c��������ȴ��33������ʱ����Na2SO3•7H2O��Ӧ�ڽϸ��¶�������Ũ���ᾧ����c����
��ѡ��b��
��5���������ȥ�������ƣ���ֹ���ţ������Ȼ�����Һ������������ӣ�
�ʴ�Ϊ��ϡ���ᡢBaCl2��Һ��
��6����IO3-��SO32-����������ԭ��Ӧ�õ�SO42-��I-��IԪ�ػ��ϼ۽���6�ۣ�SԪ�ػ��ϼ�����2�ۣ����ϼ�������С������Ϊ6���ɵ�IO3-��ϵ��Ϊ1��SO32-��ϵ��Ϊ3����ƽ�����ӷ���ʽΪ��IO3-+3SO32-=3SO42-+I-��
�ʴ�Ϊ��1��3��3SO42-��1I-��
������KIO3�����ʵ���Ϊy��10-3L��x mol/L=xy��10-3mol��
��IO3-+3SO32-=3SO42-+I-����֪n��Na2SO3��=3n��KIO3��=3xy��10-3mol
���Ʒ��Na2SO3����������Ϊ$\frac{3xy��1{0}^{-3}mol��126g/mol}{0.126g}$��100%=3xy��100%��
�ʴ�Ϊ��3xy��100%��
���� �����������Ʊ�Ϊ���壬����ѧ����ԭ���ķ������⡢���ʵķ����ᴿ��������ԭ��Ӧ�����ʺ����ⶨ��ʵ�鷽����ơ���Ϣ��ȡ��Ǩ�����õȣ���Ҫѧ���߱���ʵ�Ļ�����

| A�� | 16 | B�� | 26 | C�� | 46 | D�� | 50 |
| A�� | ��Ƽ���Ӧ��ҽ�����������������������Ѫ��֢ | |
| B�� | θ����࣬���ַ�θ�����������ʱ���ɷ���С�մ� | |
| C�� | ��ð����ͷʹʱ�����ð�˾ƥ�� | |
| D�� | ���������������ķ��ף�ע����ù�� |
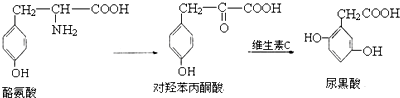
����˵��������ǣ�������
| A�� | 1mol�Ұ������뺬1molHCl�����ᷴӦ�������뺬2molNaOH����Һ��Ӧ | |
| B�� | �Ұ����ܷ����ӳɡ�ȡ������ȥ�����۷�Ӧ | |
| C�� | 1mol���DZ���ͪ��������5molH2��Ӧ | |
| D�� | 1mol�����������3molBr2��Ӧ |
| A�� | ���ԣ�KOH��NaOH | B�� | �����ԣ�Cl2��S | C�� | �ȶ��ԣ�HBr��HI | D�� | ���ԣ�H3PO4��HNO3 |
| ѡ�� | ʵ�������� | �֡������� | �ᡡ������ |
| A | T��ʱ����NaCl��NaBr�Ļ����Һ�еμ�AgNO3��Һ | �ȳ��ְ�ɫ���� | T��ʱ��Ksp�� AgCl��AgBr |
| B | ���Ũ�ȵ�Na2CO3��Һ��Na2SO4��Һ�еμӷ�̪�Լ� | Na2CO3��Һ���ɫNa2SO4��Һ���������� | �ǽ����ԣ�S��C |
| C | �����£�ȡ����CaSO4��Һ��ˮ��������ʵ�� | ��ˮʵ��ĵ��ݽ��� | CaSO4��NH3•H2O��Ϊ������� |
| D | ��Ʒ����Һ�еμ�NaClO��Һ��ͨ��SO2���� | Ʒ����Һ����Ϊ��ɫ | ���߾���Ư������ ԭ����ͬ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ӫ�⵰����һ�ָ߷��ӻ��������ܷ���ˮ�� | |
| B�� | �ô�����Һ�����������ϴ��¯�е������ | |
| C�� | ���ô���������Һ�ļ��ԶԲ;ߺͻ������� | |
| D�� | �����ŷ�PM2.5��SO2��NOX�Ȼ��γ����� |
��2��ά����C�ֳ�Ϊ����Ѫ�ᣬ������������Ҫ�Ĺ��ܣ�����������彫ʳ������ȡ�IJ������յ�Fe3+��Ϊ�����յ�Fe2+����˵��ά����C���л�ԭ�ԣ��������Ի�ԭ�ԣ���
��3��д�����пո������ʵ����ơ�������ѧʽ��
| ���� | ������ | ̼���� | ̼������ |
| ���� | ���� | С�մ� | |
| ��ѧʽ | Na2CO3 | NaHCO3 |
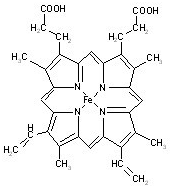 Ѫ������Ѫ�쵰�����ϵ���Ҫ�ȶ��ṹ��ΪѪ�쵰�ס����쵰�ĸ���������ӽṹ��ͼ��
Ѫ������Ѫ�쵰�����ϵ���Ҫ�ȶ��ṹ��ΪѪ�쵰�ס����쵰�ĸ���������ӽṹ��ͼ��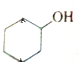 ������3������̼ԭ�ӣ�
������3������̼ԭ�ӣ�