题目内容
25℃时,水的电离达到平衡:H2O  H++OH— ΔH>0,下列叙述正确的是( )
H++OH— ΔH>0,下列叙述正确的是( )
A.向水中加入氢氧化钠,平衡逆向移动,c(H+)降低,c(OH―)增大
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大
C.向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,c(H+)不变
A
【解析】
试题分析:水的电离平衡:H2O 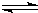 H++OH-中,要使平衡发生移动,应改变溶液c(H+)或c(OH-)的浓度,水的电离是吸热过程,升高温度,平衡向电离方向移动,K增大,c(H+),向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,c(OH-)增大,A正确;向水中加入少量固体硫酸氢钠,平衡逆向移动,c(H+)增大,c(OH-)减小,Kw只受温度的影响,温度不变,Kw不变,B错误;向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)增大,c(OH-)减小,C错误;水的电离是吸热过程,升高温度,平衡向电离方向移动,K增大,c(H+)增大,D错误。
H++OH-中,要使平衡发生移动,应改变溶液c(H+)或c(OH-)的浓度,水的电离是吸热过程,升高温度,平衡向电离方向移动,K增大,c(H+),向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,c(OH-)增大,A正确;向水中加入少量固体硫酸氢钠,平衡逆向移动,c(H+)增大,c(OH-)减小,Kw只受温度的影响,温度不变,Kw不变,B错误;向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)增大,c(OH-)减小,C错误;水的电离是吸热过程,升高温度,平衡向电离方向移动,K增大,c(H+)增大,D错误。
考点:考查弱电解质在水溶液中的电离平衡。

(20分)
(1)已知可逆反应:M(g)+N(g)P(g)+Q(g) ΔH>0,请回答下列问题:
①在某温度下,反应物的起始浓度分别为:c(M)= 1 mol·L-1,c(N)=2.4 mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为 ;
②若反应温度不变,反应物的起始浓度分别为:c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a= ;
(2)甲、乙两瓶氨水的浓度分别为1 mol·L-1和0.1 mol·L-1,则甲、乙两瓶氨水中c(OH-)之比_______(填“大于”、“小于”或“等于”)10,说明理由_____________________________ 。
(3)25℃时几种物质的电离度(溶液浓度均为0.1mol/L) 如下表(已知硫酸的第一步电离是完全的):
①H2SO4溶液: HSO4- | ②NaHSO4溶液: HSO4- | ③盐酸 HCl=H++Cl |
10% | 29% | 100% |
25℃时,0.1mol/L上述几种溶液加入完全一样的等量锌粒,反应速率从大到小的顺序
是 (填序号)
②25℃时,c(H+)相同的上述几种溶液,其物质的量浓度由大到小的顺序是 (填序号)
③25℃时,0.1mol/L H2SO4中的HSO4-的电离度小于0.1mol/L NaHSO4中HSO4-的电离度的原因是________________ 。
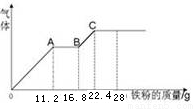
 CO2(g)+H2(g)
CO2(g)+H2(g)
 CO2(g)+H2(g)达到平衡状态的是_________
CO2(g)+H2(g)达到平衡状态的是_________ (CO)=
(CO)= (CO)=_____;
(CO)=_____; (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
(填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)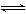 H++SO42-
H++SO42- 3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )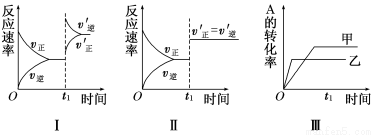
 具有相同质子数和电子数的一组是
具有相同质子数和电子数的一组是