题目内容
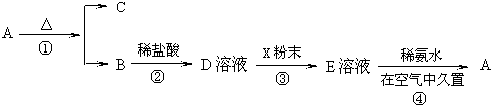
11.已知A、B、C、D 是原子序数依次增大的四种短周期元素,B 的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D 原子有2 个未成对电子.A、B、D 三种元素组成的一种化合物M 是新装修居室中常含有的一种有害气体.E 是第四周期元素,其原子核外最外层电子数与A 原子相同,其余各层电子均充满.请回答下列问题(用元素符号或化学式表示):
(1)元素B、C、D 的基态原子的第一电离能由大到小的顺序为N>O>C.
(2)M 分子中B 原子轨道的杂化类型为sp2.
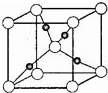
(3)E 的核外电子排布式为1s22s22p63s23p63d10,如图1是由D、E 形成的某种化合物的晶胞结构示意图,该晶体1 个晶胞中阳离子的个数为4.

(4)化合物CA3的沸点比化合物BA4的高,其主要原因是NH3分子间能形成氢键.
(5)写出与BD2互为等电子体的C3-的结构式[N=N=N]-.
(6)微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置.最早用于有机废水处理,图2是利用微生物燃料电池处理含M 废水的装置,其中3 是质子交换膜.负极所在的左室中发生反应的电极反应式是HCHO-4e-+H2O=CO2+4H+.
(7)铁粉和E 单质粉末的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO 的体积和剩余金属的质量如表(假设硝酸的还原产物只有NO).则稀硝酸的浓度为4mol/L.
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸的体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属的质量/g | 18.0 | 9.6 | 0 | 0 |
| NO 的体积/mL | 2240 | 4480 | 6720 | V |
分析 A、B、C、D是原子序数依次增大的四种短周期元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布为1s22s22p2,故B为碳元素;D原子有2个未成对电子,A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,M为HCHO,则A为H元素、D为O元素;C原子序数介于碳、氧之间,故C为N元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,核外电子排布为1s22s22p63s23p63d104s1,则E为Cu.
(1)同周期随原子序数增大,第一电离能呈增大趋势,但原子处于全满、半满、全空时,能量较低,第一电离能高于同周期相邻元素;
(2)M为HCHO,根据分子中C原子σ键数目、孤电子对数确定杂化轨道数目,进而确定杂化方式;
(3)Cu失去4s能级1个电子形成Cu+;由晶胞结构可知,Cu+位于晶胞内部;
(4)分子之间存在氢键会使物质的熔沸点升高;
(5)CO2、N3-互为等电子体,二者结构相似,N3-中N原子之间形成2对共用电子对;
(6)负极发生氧化反应,由图可知,HCHO发生氧化反应生成二氧化碳,由守恒守恒可知还生成H+;
(7)由表中数据可知,实验①②都有金属剩余,硝酸完全反应,则溶液中不可能含有硝酸铁,溶液中金属离子为+2价,在实验①的基础上加入100mL硝酸,参加反应的金属的质量为18g-9.6g=8.4g,生成NO的体积为4480mL-2240mL=2240mL,NO物质的量为0.1mol,根据电子转移守恒可知,参加反应金属的物质的量为$\frac{0.1mol×(5-2)}{2}$=0.15mol,参加反应金属的平均摩尔质量为$\frac{8.4g}{0.15mol}$=56g/mol,故该过程只有Fe参加反应,故实验①只有Fe参与反应,发生反应为:3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,根据NO的体积结合方程式计算硝酸的物质的量,进而计算硝酸的物质的量浓度.
解答 解:A、B、C、D是原子序数依次增大的四种短周期元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布为1s22s22p2,故B为碳元素;D原子有2个未成对电子,A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,M为HCHO,则A为H元素、D为O元素;C原子序数介于碳、氧之间,故C为N元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,核外电子排布为1s22s22p63s23p63d104s1,则E为Cu.
(1)同周期随原子序数增大,第一电离能呈增大趋势,但N原子2P能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:N>O>C,故答案为:N>O>C;
(2)M为HCHO,分子中C原子形成3个σ键、没有孤电子对,故杂化轨道数目为3,C原子采取sp2杂化方式,故答案为:sp2;
(3)Cu失去4s能级1个电子形成Cu+,基态核外电子排布式为1s22s22p63s23p63d10,由晶胞结构可知,Cu+位于晶胞内部,晶胞中含有4个Cu+,故答案为:1s22s22p63s23p63d10;4;
(4)NH3分子间能形成氢键,甲烷分子之间为分子间作用力,氢键比分子间作用力强,故NH3的沸点比CH4的高,故答案为:NH3分子间能形成氢键;
(5)CO2、N3-互为等电子体,二者结构相似,N3-中N原子之间形成2对共用电子对,N3-的结构式[N=N=N]-,故答案为:[N=N=N]-;
(6)负极发生氧化反应,由图可知,HCHO发生氧化反应生成二氧化碳,由守恒守恒可知还生成H+,负极所在的左室中发生反应的电极反应式是:HCHO-4e-+H2O=CO2+4H+,故答案为:HCHO-4e-+H2O=CO2+4H+;
(7)由表中数据可知,实验①②都有金属剩余,硝酸完全反应,则溶液中不可能含有硝酸铁,溶液中金属离子为+2价,在实验①的基础上加入100mL硝酸,参加反应的金属的质量为18g-9.6g=8.4g,生成NO的体积为4480mL-2240mL=2240mL,NO物质的量为0.1mol,根据电子转移守恒可知,参加反应金属的物质的量为$\frac{0.1mol×(5-2)}{2}$=0.15mol,参加反应金属的平均摩尔质量为$\frac{8.4g}{0.15mol}$=56g/mol,故该过程只有Fe参加反应,故实验①只有Fe参与反应,实验①发生反应为:3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,生成NO的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,根据方程式可知,参加反应的硝酸的物质的量为0.1mol×4=0.4mol,故硝酸的物质的量浓度为$\frac{0.4mol}{0.1L}$=4mol/L,故答案为:4.
点评 本题考查物质结构问题、混合物的有关计算、原电池原理等,(7)中根据表中数据判断各阶段发生的反应是解题关键,侧重对学生综合能力的考查,本题过程复杂、计算量较大,为易错题目,难度较大.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(2)写出Cr3+的电子排布式[Ar]3d3 ;元素周期表分为五个区域,Ga属于p区元素.
(3)Fe3+的化学性质比Fe2+稳定,其原因是Fe3+的3d轨道为半充满状态.
(4)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有5种.
(5)试比较:第一电离能I1(K)<I1(Ca)(填“>”、“<”或“=”).
| A. | p=$\frac{17V+22400}{22.422.4V}$ | B. | W=$\frac{17c}{ρ}$ | ||
| C. | $\frac{17V}{17V+22400}$=W | D. | C=$\frac{1000Vρ}{17V+22400}$ |
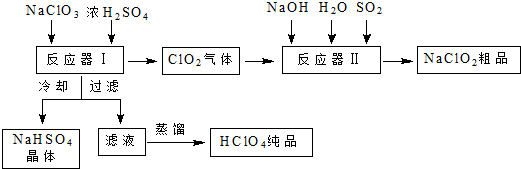
 甲烷在一定条件下可生成以下微粒:
甲烷在一定条件下可生成以下微粒:
 .
.