题目内容
11.下列关于化学反应与能量的说法不正确的是( )| A. | 化学反应必然伴随发生能量变化 | |
| B. | 化学反应中的能量变化主要是由化学键变化引起的 | |
| C. | 反应物的总能量与生成物的总能量一定相等 | |
| D. | 化学反应中既有物质变化又有能量变化 |
分析 A、化学反应中能量守恒、质量守恒;
B、化学变化中的能量变化主要是由旧键的断裂和新键的形成;
C、化学反应中有物质变化一定伴随有能量变化;
D、化学反应中有物质变化一定伴随有能量变化.
解答 解:A、因化学反应中能量守恒,所以化学反应必然伴随发生能量变化,故A正确;
B、因化学变化中的能量变化主要原因是由旧键的断裂和新键的形成,故B正确;
C、化学反应中有物质变化一定伴随有能量变化,即反应物总能量与生成物总能量一定不相等,故C错误;
D、化学反应中有物质变化一定伴随有能量变化,故D正确,
故选C.
点评 本题考查了化学反应能量变化的原因,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
13.碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如图:
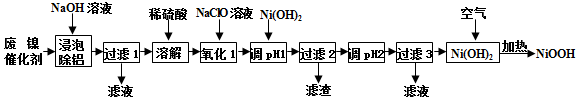
回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(2)“溶解”时放出的气体为H2、H2S (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
“调pH=1”时,溶液pH范围为5.6~6.2;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式4Ni(OH)2+O2$\frac{\underline{\;\;△\;\;}}{\;}$4NiOOH+2H2O;
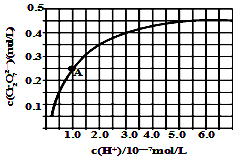
(5)金属铬在溶液中有多种存在形式,CrO42-和Cr2O72-在溶液中可相互转化.室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应2CrO42-+2H+?Cr2O72-+H2O,根据A点数据计算出该转化反应的平衡常数为1014,温度升高,溶液中CrO42-的平衡转化率减小,则该反应的△H<0(填“>”、“<”或“=”).

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(2)“溶解”时放出的气体为H2、H2S (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 开始沉淀的pH | 完全沉淀的pH | |
| Ni2+ | 6.2 | 8.6 |
| Fe2+ | 7.6 | 9.1 |
| Fe3+ | 2.3 | 3.3 |
| Cr3+ | 4.5 | 5.6 |
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式4Ni(OH)2+O2$\frac{\underline{\;\;△\;\;}}{\;}$4NiOOH+2H2O;
(5)金属铬在溶液中有多种存在形式,CrO42-和Cr2O72-在溶液中可相互转化.室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应2CrO42-+2H+?Cr2O72-+H2O,根据A点数据计算出该转化反应的平衡常数为1014,温度升高,溶液中CrO42-的平衡转化率减小,则该反应的△H<0(填“>”、“<”或“=”).

11.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是( )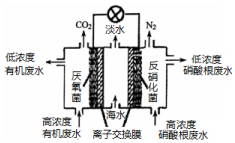

| A. | 该电池能在高温下工作 | |
| B. | 该电池工作时,中间室中的Cl-移向右室 | |
| C. | 正极上发生的电极反应:2NO3-+6H2O+10e-═N2↑+12OH- | |
| D. | 若有机废水中有机物用C6H12O6表示,每消耗1 mol C6H12O6转移4 mol电子 |
16.下列叙述不正确的是( )
| A. | 100℃纯水的pH<7,此时水仍呈中性 | |
| B. | pH=3的醋酸溶液,稀释至100倍后pH小于5 | |
| C. | 0.2 mol/L的盐酸,与等体积水混合后pH=1 | |
| D. | pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7 |
3.12.8gCu与足量浓硝酸反应,铜完全反应后,产生气体在标况下的体积为 4.48L,则消耗硝酸的物质的量为( )
| A. | 0.20mol | B. | 0.40mol | C. | 0.42mol | D. | 0.60m |
20.H2(g)+I2(g)?2HI(g)△H=-Q(Q>0),下列说法正确的是( )
| A. | 温度升高,反应速率增大,产率增大 | |
| B. | 增大反应物H2的浓度,HI%增大 | |
| C. | 增大压强,浓度增大,平衡不移动 | |
| D. | 使用催化剂,反应速率增大,I2的转化率增大 |