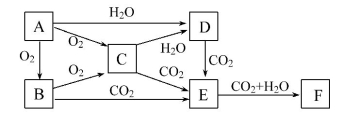
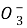题目内容
把SO2通入NaOH溶液中,当SO2和NaOH完全反应时,其质量比为6∶5,则下列说法正确的是 ( )
A.反应后SO2有剩余
B.溶液还可吸收SO2
C.溶液中除OH-外,只存在一种阴离子
D.溶液中溶质(正盐与酸式盐)的物质的量之比为1∶2
B、D
【解析】
试题分析: SO2通入NaOH溶液可以发生如下反应:SO2+2NaOH(过量)====Na2SO3+H2O、SO2(过量)+NaOH====NaHSO3。当n(NaOH)∶n(SO2)=2∶1时,反应后生成Na2SO3,当n(NaOH)∶n(SO2)=1∶1时,反应后生成NaHSO3,当1∶1<n(NaOH)∶n(SO2)<2∶1时,反应后生成NaHSO3和Na2SO3。因为n(NaOH)∶n(SO2)=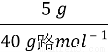 ∶
∶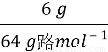 =4∶3,介于1∶1和1∶2之间,所以产物是NaHSO3和Na2SO3。反应物是SO2和OH-,生成物是S
=4∶3,介于1∶1和1∶2之间,所以产物是NaHSO3和Na2SO3。反应物是SO2和OH-,生成物是S 、HS
、HS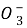 和H2O,据此可以写出如下离子方程式3SO2+4OH-
和H2O,据此可以写出如下离子方程式3SO2+4OH- S
S +2HS
+2HS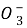 +H2O。SO2和NaOH溶液都没有剩余,A选项错误;产物中有Na2SO3还可以继续吸收SO2:Na2SO3+SO2+H2O
+H2O。SO2和NaOH溶液都没有剩余,A选项错误;产物中有Na2SO3还可以继续吸收SO2:Na2SO3+SO2+H2O 2NaHSO3,B选项正确;溶液中含有S
2NaHSO3,B选项正确;溶液中含有S 、HS
、HS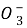 和OH-三种阴离子,C选项错误;根据方程式可以看出,n(S
和OH-三种阴离子,C选项错误;根据方程式可以看出,n(S )∶n(HS
)∶n(HS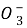 )=1∶2,D选项正确。
)=1∶2,D选项正确。
考点:二氧化硫的性质和作用

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
 、OH-、N
、OH-、N ,则溶液中可能存在的离子有 ,一定存在的离子有 ,一定不存在的离子有 ,反应的离子方程式为 。
,则溶液中可能存在的离子有 ,一定存在的离子有 ,一定不存在的离子有 ,反应的离子方程式为 。
 ( )
( )