题目内容
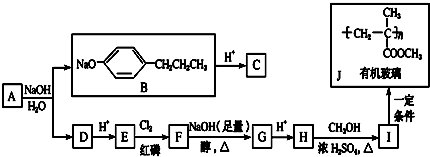
15.DAP-A树脂(下列路线图中的β、γ聚合物)是一种优良的热固性树脂,被用作高级UV油墨的一种成分.用UV油墨印刷的优点是:印刷时油墨极快干燥,对环境及人员无损害,性价比较高.因此,适于大规模生产食品、酒类、洗涤剂等包装纸盒.以下是以石油化工产品为原料,合成该材料的路线: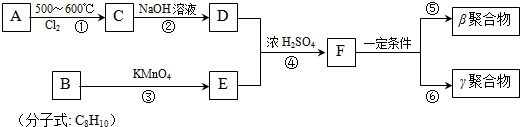
已知:
Ⅰ.
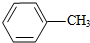 $\stackrel{MnO_{4}}{→}$
$\stackrel{MnO_{4}}{→}$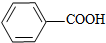
Ⅱ.RCH2CH=CH2+Cl2$\stackrel{500-600℃}{→}$
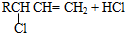 =CH2+HCl
=CH2+HClⅢ.β聚合物的结构简式:

试回答下列问题:
(1)A的名称是CH2=CH-CH3.
(2)在①~④的反应中属于取代反应的是①②④.
(3)B的结构简式是
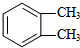 ,B苯环上的二氯代物的结构简式为:
,B苯环上的二氯代物的结构简式为: ,
,(4)写出反应④的化学方程式:
 .
.(5)工业上可由C经过两步反应制得甘油(丙三醇),写出第一步的反应类型及第二步反应的化学方程式:加成反应、
 .
.(6)γ聚合物和β聚合物相比,下列说法合理的是BC.
A.它们互为同分异构体 B.它们含碳的质量分数相同
C.γ聚合物中可能几乎不含碳碳双键D.不能发生水解反应.
分析 由β聚合物的结构简式可确定F为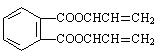 ,由转化关系可知,B发生信息Ⅰ反应生成E,E应为羧酸,结合F的结构可推出E为
,由转化关系可知,B发生信息Ⅰ反应生成E,E应为羧酸,结合F的结构可推出E为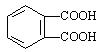 ,B为
,B为 ,则D为CH2=CH-CH2-OH,逆推可知C为CH2=CH-CH2-Cl、A为CH2=CH-CH3,A发生取代反应生成C,C发生水解反应生成D,D和E发生酯化反应生成F,据此分析解答.
,则D为CH2=CH-CH2-OH,逆推可知C为CH2=CH-CH2-Cl、A为CH2=CH-CH3,A发生取代反应生成C,C发生水解反应生成D,D和E发生酯化反应生成F,据此分析解答.
解答 解:由β聚合物的结构简式可确定F为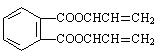 ,由转化关系可知,B发生信息Ⅰ反应生成E,E应为羧酸,结合F的结构可推出E为
,由转化关系可知,B发生信息Ⅰ反应生成E,E应为羧酸,结合F的结构可推出E为 ,B为
,B为 ,则D为CH2=CH-CH2-OH,逆推可知C为CH2=CH-CH2-Cl、A为CH2=CH-CH3,A发生取代反应生成C,C发生水解反应生成D,D和E发生酯化反应生成F,
,则D为CH2=CH-CH2-OH,逆推可知C为CH2=CH-CH2-Cl、A为CH2=CH-CH3,A发生取代反应生成C,C发生水解反应生成D,D和E发生酯化反应生成F,
(1)通过以上分析知,A为CH2=CH-CH3,名称是丙烯,故答案为:丙烯;
(2)在①~④的反应中属于取代反应的是①②④,故答案为:①②④;
(3)B的结构简式为 ,B苯环上二氯代物结构简式为
,B苯环上二氯代物结构简式为
故答案为: ;
;
(4)反应④的化学方程式为: ,
,
故答案为: ;
;
(5)C可以由两步反应生成丙三醇,第一步为丙烯的加成反应,然后是1,2,3-三氯丙烷的取代反应,
第二步反应方程式为为: ,
,
故答案为:加成反应; ;
;
(6)γ聚合物和β聚合物相比,
A.二者链节不能,它们不是同分异构体,故A错误;
B.二者最简式相同,它们含碳的质量分数相同,故B正确;
C.F中碳碳双键均发生加聚反应得到γ聚合物,故γ聚合物中几乎不含碳碳双键,故C正确;
D.二者链节中都含有酯基,可以发生水解反应,故D错误,
故选:BC.
点评 本题考查有机物推断,为高频考点,侧重考查学生推断及信息迁移能力,利用反应条件、某些物质结构简式、题给信息进行推断,注意:连接苯环的碳原子上含有氢原子的苯的同系物都能被酸性高锰酸钾溶液氧化生成-COOH,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 编号 | 实验内容 | 实验目的 |
| A | 分别将一小粒钠投入水与无水乙醇中,钠与水反应更剧烈 | 证明羟基氢活泼性: H2O>C2H5OH |
| B | 向滴有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液,溶液褪色 | 证明溴乙烷发生消去反应有乙烯生成 |
| D | 测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
| A. | 碳酸钙溶于稀硝酸:CO32-+2H+→CO2↑+H2O | |
| B. | 氯化铜溶液中加入NaHS溶液:Cu2++HS-=CuS↓+H+ | |
| C. | 碳酸钠溶液中通入少量二氧化碳:CO32-+CO2+H2O=2HCO3- | |
| D. | 硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-→NH3↑+H2O |
| A. | 标准状况下,2.24 L己烷含有分子的数目为0.1NA | |
| B. | 原子结构示意图: 表示12C,也可以表示13C 表示12C,也可以表示13C | |
| C. | 0.1 mol/L Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| D. | 由离子方程式□□+XO3-+6H+=3X2+3H2O可判断X元素的最高化合价为+5价 |
| A. | $\frac{W}{m+n+2}$×m mol | B. | $\frac{W}{m+n}$×m mol | C. | $\frac{W}{m+n+2}$×(m+2)mol | D. | $\frac{W}{m+n}$×(m-2)mol |
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A. | 2NaClO+CO2+H2O→Na2CO3+2HClO | |
| B. | HCN+Na2CO3→NaHCO3+NaCN | |
| C. | 结合质子能力由强到弱的顺序为:CO32->HCO3->CH3COO- | |
| D. | 常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN) |
 硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:
硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
(2)将硫酸铜晶体加热到258~680℃生成的物质A,A是CuSO4(化学式);A溶于水配成溶液,加入氨水,观察到的现象是首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色溶液;最终得到溶液中的含铜元素的离子是[Cu(NH3)4]2+(化学式),该离子含有的化学键类型有配位键、极性键.
(3)将硫酸铜晶体加热到1000℃以上生成的物质C,在C中的铜的离子的基态电子排布式是1s22s22p63s22p63d10;
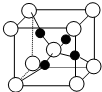
(4)如图是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子).
①该温度是1000℃以上.
②铜原子的配位数是2.
③已知该晶体的密度为dg•cm-3,则晶胞参数是$\root{3}{\frac{288}{{N}_{A}d}}$×1010pm.
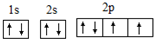 ;氧元素原子核外有3种不同能级的电子;
;氧元素原子核外有3种不同能级的电子;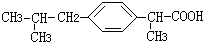
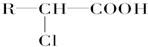 +HCl
+HCl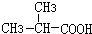 、G
、G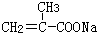 .
.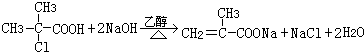 ;H→I
;H→I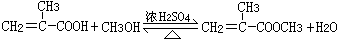 .
.