题目内容
向100mL FeBr2的溶液中,通入3molCl2.反应后溶液中Br-和Cl-的物质的量浓度相等,则溶液中发生反应的离子方程式为( )
| A、2Fe2++Cl2═2Fe3++2Cl- |
| B、2Br-+Cl2═Br2+2Cl- |
| C、4Fe2++2Br-+3Cl2═Br2+4Fe3++6Cl- |
| D、2Fe2++4Br-+3Cl2═2Br2+2Fe3++6Cl- |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:由于亚铁离子的还原性强于溴离子的,所以氯气首先氧化亚铁离子,设FeBr2的物质的量是x,则由于反应后溶液中Br-和Cl-的物质的量浓度相等,所以x+(2x-6)=6,解得x=4,以此可确定反应的离子方程式.
解答:
解:向100mL FeBr2的溶液中,通入3molCl2.因还原性Fe2+>Br-,所以氯气首先氧化Fe2+,设FeBr2的物质的量是x,则由于反应后溶液中Br-和Cl- 的物质的量浓度相等,
则反应中Fe2+全部被氧化,有(2x-6)molBr-被氧化,由氧化剂和还原剂得失电子数目相等可知,x+(2x-6)=6,解得x=4,
所以反应的离子方程式应为4Fe2++2Br-+3Cl2═Br2+4Fe3++6Cl-,
故选C.
则反应中Fe2+全部被氧化,有(2x-6)molBr-被氧化,由氧化剂和还原剂得失电子数目相等可知,x+(2x-6)=6,解得x=4,
所以反应的离子方程式应为4Fe2++2Br-+3Cl2═Br2+4Fe3++6Cl-,
故选C.
点评:本题考查氧化还原反应的相关计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意如果同一种氧化剂能和不同的还原剂混合,氧化剂首先氧化还原性最强的还原剂,其次在计算时应该利用好电子的得失守恒,难度中等.

练习册系列答案
相关题目
下列实验操作或事故处理中,做法不正确的是( )
| A、不慎将酸溅入眼中,立即用水冲洗,边洗边眨眼睛 |
| B、不慎将碱液沾到皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 |
| C、不慎碰翻酒精灯导致失火,马上用湿抹布扑灭 |
| D、稀释浓硫酸时,先把浓硫酸注入量筒,然后向其中加入水,边加边搅拌 |
下列说法正确的是( )
| A、铜、酒精、冰醋酸分别属于非电解质、电解质、弱电解质 |
| B、煤的干馏、煤的液化都属于物理变化 |
| C、Fe(OH)3胶体和CuSO4溶液都是混合物 |
| D、冰醋酸、碱式碳酸铜、小苏打分别属于酸、碱、盐 |
氢化钠是一种离子化合物,它跟水反应时生成氢氧化钠和氢气,反应方程式为NaH+H2O═NaOH+H2↑,将氢化钠和铝粉的混合物mg与足量的水充分反应后,若收集到ng氢气,则混合物中的铝的质量为( )
| A、(36n-3m)g |
| B、(m-4.8n)g |
| C、(12n-m)g |
| D、(24m-5n)g |
把a、b、c、d四种金属片浸泡在稀H2SO4中,用导线两两相连可以组成各种原电池.若a、b相连时,a为负极;c、d相连时,d为正极;a、c相连时,c上有气泡放出;b、d相连时,电子沿导线由d极流向b极.则这四种金属活动性顺序由大到小为( )
| A、a>b>c>d |
| B、a>c>d>b |
| C、c>a>b>d |
| D、b>d>c>a |
能溶于水,能发生水解反应,还能发生银镜反应的是( )
| A、淀粉 | B、麦芽糖 |
| C、葡萄糖 | D、甲酸甲酯 |
将钠放置在空气中,是生成白色的Na2O还是淡黄色的Na2O2,主要取决于下列因素中的( )
| A、反应温度 | B、空气的量 |
| C、钠粒的大小 | D、钠的形状 |
 ,则该化合物的结构简式可能是(4种):
,则该化合物的结构简式可能是(4种):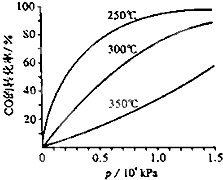 Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.