题目内容
10.NA表示阿伏加德罗常数,下列判断正确的是( )| A. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| B. | 常温常压下,22.4LCO2中含有的CO2分子数小于NA个 | |
| C. | 等物质的量的N2和CO的质量均为28g | |
| D. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA |
分析 A、溶液体积不明确;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、氮气和CO的物质的量不明确;
D、求出二氧化碳的物质的量,然后根据当1mol二氧化碳参与反应时,反应转移1mol电子.
解答 解:A、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L二氧化碳的物质的量小于1mol,故分子个数小于NA个,故B正确;
C、氮气和CO的物质的量不明确,故质量不一定是28g,故C错误;
D、标况下5.6L二氧化碳的物质的量为0.25mol,而当1mol二氧化碳参与反应时,反应转移1mol电子,故0.25mol二氧化碳反应时转移0.25NA个电子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
12.某学生的实验报告所列出的下列数据中合理的是( )
| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用托盘天平称量25.20g NaCl | |
| D. | 用25mL碱式滴定管量取碱溶液21.70mL |
18.水溶液中能大量共存的一组离子是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+ H+ SO42- HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、NH4+、NO3-、OH- |
5.在一饱和AgCl水溶液(含有AgCl固体)中,添加下列试剂能使c(Cl-)增加的是( )
| A. | 氨水 | B. | 硝酸 | C. | 水 | D. | AgNO3 |
15.下面列出了电解不同物质的电极反应式,其中错误的是( )
| A. | 用铜电极电解CuSO4溶液 阳极:Cu-2e-=Cu2+ | |
| B. | 电镀铜时(电解质溶液为CuSO4溶液) 阳极:Cu2++2e-=Cu | |
| C. | 电解熔融NaCl 阴极:Na++e-=Na | |
| D. | 电解NaOH溶液 阳极:4OH--4e-=2H2O+O2↑ |
2.下列溶液中的离子一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、SO32- | |
| B. | 室温下,由水电离出来的c(H+)=1×10-14mol•L-1的溶液中:Ba2+、NO3-、K+、ClO- | |
| C. | 能使酚酞变红色的溶液中:Na+、K+、AlO2-、CO32- | |
| D. | 含大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
19.已知a是一种常见单质,可发生如图所示的转化关系,则下列叙述中不正确的是( )
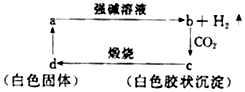

| A. | a在与强碱溶液的反应中氧化剂是强碱 | |
| B. | 向b中滴加适量盐酸可得到c | |
| C. | c不一定是两性物质 | |
| D. | d一定能和氢氧化钠溶液反应 |