题目内容
元素的原子在分子中吸引电子的能力可以用电负性X表示.下表是某些短周期元素的X值:
(1)根据表中数据归纳元素的电负性与原子吸引电子的能力的关系 .
(2)试推测,周期表所列元素中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物电子式为 .
(3)若NCl3最初水解产物是NH3和HClO,其化学方程式为NCl3+H2O=NH3+HClO,则X(Cl)的最小范围: <X(Cl)< (填表中数值);若已知X(P)<X(Cl),则PCl3水解的化学反应方程式是 .
| 元素符号 | Li | Be | B | C | N | O | F | Na | Mg | Al | P | S |
| X值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.04 | 3.44 | 3.98 | 0.93 | 1.31 | 1.61 | 2.19 | 2.58 |
(2)试推测,周期表所列元素中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物电子式为
(3)若NCl3最初水解产物是NH3和HClO,其化学方程式为NCl3+H2O=NH3+HClO,则X(Cl)的最小范围:
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:(1)元素的非金属性越强,其得电子能力越强,所以原子吸引电子能力越强,据此判断元素电负性与原子吸引电子能力关系;
(2)根据表中数据知,同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减小,所以元素周期表中除了放射性元素外,电负性最小的元素是Cs元素、电负性最大的元素是F,二者形成的化合物是离子化合物CsF;
(3)在化合物中,化合价为正的元素电负性小于化合价为负的元素电负性,同一周期元素,元素电负性随着原子序数增大而增大,据此判断Cl元素电负性;化合物发生水解反应时其元素化合价不变,据此判断PCl3水解产物.
(2)根据表中数据知,同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减小,所以元素周期表中除了放射性元素外,电负性最小的元素是Cs元素、电负性最大的元素是F,二者形成的化合物是离子化合物CsF;
(3)在化合物中,化合价为正的元素电负性小于化合价为负的元素电负性,同一周期元素,元素电负性随着原子序数增大而增大,据此判断Cl元素电负性;化合物发生水解反应时其元素化合价不变,据此判断PCl3水解产物.
解答:
解:(1)根据表中数据知,元素的非金属性越强,其电负性越大,原子吸引电子能力越强,故答案为:元素的电负性越大,原子吸引电子的能力越强;
(2)根据表中数据知,同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减小,所以元素周期表中除了放射性元素外,电负性最小的元素是Cs元素、电负性最大的元素是F,二者形成的化合物是离子化合物CsF,其电子式为 ,故答案为:
,故答案为: ;
;
(3)若NCl3最初水解产物是NH3和HClO,其化学方程式为NCl3+H2O=NH3+HClO,水解反应中各元素化合价不变,所以N元素化合价为-3价、Cl元素化合价为+1价,则N元素吸引电子能力大于Cl元素,N电负性大于Cl元素,同一周期元素,元素电负性随着原子序数增大而增大,所以S元素电负性小于Cl元素,则X(Cl)的最小范围:2.58<X(Cl)<3.04;
PCl3中P元素电负性小于Cl元素,所以该化合物中P元素化合价为+3价、Cl元素化合价为-1价,则PCl3水解产物是HCl、H3PO3,则该水解方程式为PCl3+3H2O=3HCl+H3PO3(或P(OH)3),故答案为:2.58;3.04;PCl3+3H2O=3HCl+H3PO3(或P(OH)3).
(2)根据表中数据知,同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减小,所以元素周期表中除了放射性元素外,电负性最小的元素是Cs元素、电负性最大的元素是F,二者形成的化合物是离子化合物CsF,其电子式为
 ,故答案为:
,故答案为: ;
; (3)若NCl3最初水解产物是NH3和HClO,其化学方程式为NCl3+H2O=NH3+HClO,水解反应中各元素化合价不变,所以N元素化合价为-3价、Cl元素化合价为+1价,则N元素吸引电子能力大于Cl元素,N电负性大于Cl元素,同一周期元素,元素电负性随着原子序数增大而增大,所以S元素电负性小于Cl元素,则X(Cl)的最小范围:2.58<X(Cl)<3.04;
PCl3中P元素电负性小于Cl元素,所以该化合物中P元素化合价为+3价、Cl元素化合价为-1价,则PCl3水解产物是HCl、H3PO3,则该水解方程式为PCl3+3H2O=3HCl+H3PO3(或P(OH)3),故答案为:2.58;3.04;PCl3+3H2O=3HCl+H3PO3(或P(OH)3).
点评:本题考查元素电负性含义及应用,侧重考查学生分析、归纳能力,注意把握元素周期律内容,注意理解电负性意义及应用,难点是(3)题水解产物判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
工业上用洗净的废铜屑作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 | |||||
| B、Cu+HNO3(稀)→Cu(NO3)2 | |||||
C、Cu
| |||||
D、Cu
|
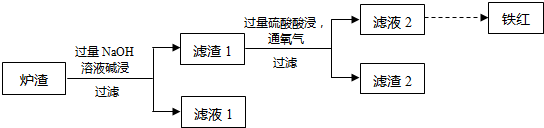
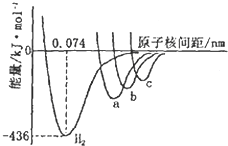 X元素在第3周期中电负性最大,Y、Z元素同主族且位置相邻,Y原子的最外层电子排布为nsnnpn+2.请填写下列空白.
X元素在第3周期中电负性最大,Y、Z元素同主族且位置相邻,Y原子的最外层电子排布为nsnnpn+2.请填写下列空白.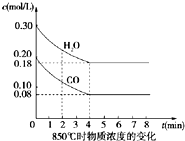 在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应:
在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应: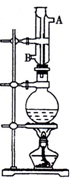 实验室利用如图中装置制取乙酸异戊酯,其合成过程为:
实验室利用如图中装置制取乙酸异戊酯,其合成过程为: