题目内容
已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体.根据下列关系,试回答:
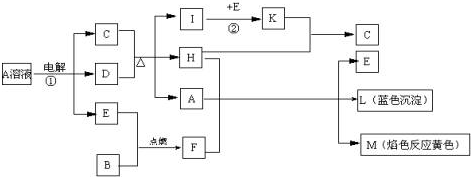
(1)L的化学式: F的电子式: .
(2)反应①的离子方程式: .
(3)反应②,工业上采取的反应条件: .
(4)每生成1molK,反应放出98.3kJ热量,该反应的热化学方程式为: .

(1)L的化学式:
(2)反应①的离子方程式:
(3)反应②,工业上采取的反应条件:
(4)每生成1molK,反应放出98.3kJ热量,该反应的热化学方程式为:
考点:无机物的推断
专题:推断题
分析:A的电解产物反应生成H,H常温下为无色液体,H为H2O;L是蓝色沉淀,为Cu(OH)2,M的焰色反应为黄色,M含有Na元素,由转化关系A+H+F→E+L+M,即A溶液+F→E+L+M,可知F与水反应生成碱与E,且B+E→F,故F为Na2O2,E为O2,B为金属Na,A为铜盐,由A溶液
C+D+E可知,电解产物为三种,为放氧生酸型,电解生成Cu、O2、酸,C的浓溶液在加热时与D反应,D为Cu,C为H2SO4,故A为CuSO4,由C+D
I+D+H可知,I为SO2,由I
K可知,K为SO3,SO3与水反应生成硫酸,验证符合转化关系.
| 电解 |
| △ |
| E |
解答:
解:A的电解产物反应生成H,H常温下为无色液体,H为H2O;L是蓝色沉淀,为Cu(OH)2,M的焰色反应为黄色,M含有Na元素,由转化关系A+H+F→E+L+M,即A溶液+F→E+L+M,可知F与水反应生成碱与E,且B+E→F,故F为Na2O2,E为O2,B为金属Na,A为铜盐,由A溶液
C+D+E可知,电解产物为三种,为放氧生酸型,电解生成Cu、O2、酸,C的浓溶液在加热时才与D反应,D为Cu,C为H2SO4,故A为CuSO4,由C+D
I+D+H可知,I为SO2,由I
K可知,K为SO3,SO3与水反应生成硫酸,验证符合转化关系.
(1)由想上述分析可知,L是蓝色沉淀为Cu(OH)2,F为Na2O2,电子式为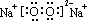 ,故答案为:Cu(OH)2;
,故答案为:Cu(OH)2;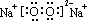 ;
;
(2)反应①为电解硫酸铜溶液生成铜、硫酸、氧气,反应离子方程式为:2Cu2++2H2O
2Cu+O2↑+4H+,
故答案为:2Cu2++2H2O
2Cu+O2↑+4H+;
(3)反应②是二氧化硫被氧气氧化为三氧化硫,工业上釆取的反应条件是:常压、催化剂、400℃~500℃,
故答案为:常压、催化剂、400℃~500℃;
(4)每生成1molK为SO3,反应放出98.3kJ热量,该反应的热化学方程式为:SO2(g)+
O2(g)?SO3(g)△H=-98.3kJ/mol,
故答案为:SO2(g)+
O2(g)?SO3(g)△H=-98.3kJ/mol.
| 电解 |
| △ |
| E |
(1)由想上述分析可知,L是蓝色沉淀为Cu(OH)2,F为Na2O2,电子式为
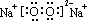 ,故答案为:Cu(OH)2;
,故答案为:Cu(OH)2;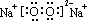 ;
;(2)反应①为电解硫酸铜溶液生成铜、硫酸、氧气,反应离子方程式为:2Cu2++2H2O
| ||
故答案为:2Cu2++2H2O
| ||
(3)反应②是二氧化硫被氧气氧化为三氧化硫,工业上釆取的反应条件是:常压、催化剂、400℃~500℃,
故答案为:常压、催化剂、400℃~500℃;
(4)每生成1molK为SO3,反应放出98.3kJ热量,该反应的热化学方程式为:SO2(g)+
| 1 |
| 2 |
故答案为:SO2(g)+
| 1 |
| 2 |
点评:本题以无机框图题的形式考查Na、S、Cu等元素单质及其化合物之间的相互转化关系和逻辑推理能力、化学用语的书写、硫酸工业等,本题中L是蓝色沉淀,M的焰色反应为黄色,H常温下为无色液体以及A的电解等为解题突破口,根据L、M推断出F、E,再利用倒推法与顺推法向结合推断,对学生的逻辑推理能力提出较高要求,题目难度较大.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)?2Z(g)+W(s);下列不能判断达到化学平衡状态的标志是( )
| A、混合气体的平均摩尔质量不变 |
| B、当容器中气体压强不变 |
| C、生成2mol Z的同时生成1mol X |
| D、混合气体的密度不变 |
下列各组气体中,在通常情况下既能用浓硫酸又能用碱石灰干燥的有( )
| A、H2S、O2、N2 |
| B、HCl、Cl2、CO2 |
| C、N2、H2、CO |
| D、SO2、Cl2、O2 |
化学与生活密切相关,下列说法不正确的是( )
| A、二氧化硫可用于漂白纸浆 |
| B、向燃煤中添加石灰石可减少SO2的排放 |
| C、碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 |
| D、氮是生命体内不可缺少的元素,但多数生物不能直接从空气中吸收氮气 |
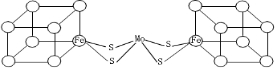 .图中左右两边对称,各含一个近似立方体的结构.每个立方体含有4个Fe原子和4个S原子,它们位于立方体的8个顶点,且原子间只有一种化学键.
.图中左右两边对称,各含一个近似立方体的结构.每个立方体含有4个Fe原子和4个S原子,它们位于立方体的8个顶点,且原子间只有一种化学键.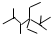 的名称是
的名称是 的名称为
的名称为
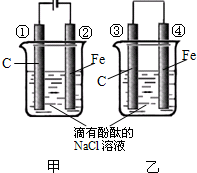 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.