题目内容
18.下列说法正确的是( )| A. | 能使润湿的淀粉KI试纸变成蓝色的气体一定是Cl2 | |
| B. | 为除去FeCl2溶液中少量的FeCl3,可加入过量铁粉,再过滤 | |
| C. | 用稀氨水能鉴别Al(N03)3、Mg(NO3)2、KNO3三种溶液 | |
| D. | 向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42- |
分析 A、具有氧化性的气体能够使润湿的淀粉KI试纸变成蓝色;
B、除杂过程中不能引入新的杂质,所加的试剂只跟杂质反应,不能与主体物质反应;
C、稀氨水不能鉴别Al(N03)3、Mg(NO3)2,两者现象相同都生成白色沉淀;
D、硝酸具有强氧化性,可将亚硫酸钡沉淀氧化成硫酸钡.
解答 解:A、某气体能能使润湿的淀粉KI试纸变成蓝色,说明该气体的氧化性大于碘单质,可以为O3、NO2等强氧化性气体,不一定是Cl2,故A错误;
B、加铁粉发生Fe+2Fe3+=3Fe2+,除去了杂质,生成主体物质,故B正确;
C、氢氧化铝不溶于弱碱,所以稀氨水不能鉴别Al(N03)3、Mg(NO3)2,两者现象相同都生成白色沉淀,故C错误;
D、硝酸钡加稀盐酸形成了硝酸,硝酸具有强氧化性,可将亚硫酸钡沉淀氧化成硫酸钡,则原溶液中有SO32-或SO42-均符合,故D错误;
故选B.
点评 本题考查了离子检验的方法和现象分析,掌握常见离子的检验方法,注意干扰离子的判断.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
8.在密闭容器中发生反应:aX(g)+bY(g)?cZ(g)+dW(g),反应达平衡后保持温度不变,将气体体积压缩到原来的一半,当再次达平衡时,W的浓度为原平衡时的1.7倍.下列叙述中不正确( )
| A. | 平衡向逆反应方向移动 | B. | a<c+d | ||
| C. | Z的体积分数增加 | D. | X的转化率下降 |
9.下列除去杂质的操作方法错误的是( )
| A. | 氧化镁中含少量氧化铝:加足量氧氧化钠溶液充分搅拌后过滤 | |
| B. | 氢气中含少量氯化氢:通入装有氢氧化钠的洗气瓶 | |
| C. | 自来水中含少量Fe3+、蒸馏 | |
| D. | 硝酸钾固体中含少量氧化钾:配制80℃的饱和溶液,冷却、结晶、过滤、洗涤、干燥 |
6.下列与实验相关的说法正确的是( )
| A. | 向碘水中加入有机溶剂提取碘,只能从分液漏斗下口分离出含碘的有机层 | |
| B. | 加入稀盐酸产生无色气体,通入品红溶液不褪色,原溶液中一定含CO32-或HCO3- | |
| C. | 在容量瓶定容时,仰视刻度线滴加蒸馏水,则配制溶液的物质的量浓度偏小 | |
| D. | 进行酸碱中和滴定时,眼睛要始终注视滴定管液面高度的变化 |
13.我国的四大发明之一黑火药,爆炸时的主要反应是:S+2KNO3+3C═K2S+3CO2↑+N2↑,下列说法不正确的是( )
| A. | 每生成0.5 mol N2,反应中转移6 mol电子 | |
| B. | 硝酸钾、硫磺在黑火药爆炸的反应中是氧化剂 | |
| C. | KNO3有强氧化性,乘坐汽车、火车、飞机时不能随身携带 | |
| D. | 上述反应的生成物都是无毒的,所以燃放爆竹时不会污染环境 |
3.下列图示实验能达到实验目的是( )
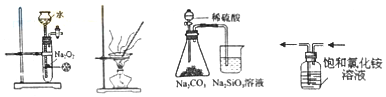

| A. | 制备少量O2 | B. | 制备无水氯化铁 | ||
| C. | 比较元素非金属性强弱 | D. | 收集氨气 |
10.以下物质间的转化不能通过一步反应实现的是( )
| A. | HClO→O2 | B. | Cu→CuSO4 | C. | CO2→CaCO3 | D. | Al2O3→Al(OH)3 |