题目内容
在相同条件下,下列三个化学反应反应热分别以△H1、△H2、△H3表示,
(1)2H2(g)+O2(g)=2H2O(g);△H1
(2)2H2(g)+O2(g)=2H2O(1);△H2
(3)H2(g)+O2(g)═H2O(g);△H3,
则△H1、△H2和△H3的关系是( )
(1)2H2(g)+O2(g)=2H2O(g);△H1
(2)2H2(g)+O2(g)=2H2O(1);△H2
(3)H2(g)+O2(g)═H2O(g);△H3,
则△H1、△H2和△H3的关系是( )
分析:由于气态水的能量高于液态水的能量,所以氢气燃烧生成液态水放出的热量多,但放热越多,△H越小;反应热和方程式中物质前面的计量数成正比;
解答:解:根据气态水的能量高于液态水的能量,所以氢气燃烧生成液态水放出的热量多,但放热越多,△H越小,所以△H1>△H2,反应热和方程式中物质前面的计量数成正比,所以△H1=2△H3,
故选:B;
故选:B;
点评:本题考查了反应热的大小比较,注意比较反应热时不能忽略“+”“-”.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
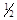 O2(g)==H2O(g);△H3 ,则△H1、△H2和△H3的关系是
O2(g)==H2O(g);△H3 ,则△H1、△H2和△H3的关系是