题目内容
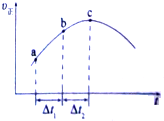 自一个恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示.由此得出结论正确的是( )
自一个恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示.由此得出结论正确的是( )| A、反应物浓度:a点小于c点 |
| B、△t1=△t2时氢气的产率:ab段小于bc段 |
| C、该反应的正反应为吸热反应 |
| D、c点反应进行的程度最大 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:由题意可知一个反应前后体积不变的可逆反应,由于容器恒容,因此压强不影响反应速率,所以在本题中只考虑温度和浓度的影响.结合图象可知反应速率先增大再减小,因为只要开始反应,反应物浓度就要降低,反应速率应该降低,但此时正反应却是升高的,这说明此时温度的影响是主要的,因此只能是放热反应,从而导致容器内温度升高反应速率加快.
解答:
解:A、a到c时正反应速率增加,反应物浓度随时间不断减小,起始时反应物浓度最大,故A错误;
B、随着反应的进行,正反应速率越快,生成氢气的产率将逐渐增大,△t1=△t2时,H2的产率:a~b段小于b~c段,故B正确;
C、从a到c正反应速率增大,之后正反应速率减小,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,说明该反应为放热反应,故C错误;
D、化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,故D错误;
故选:B.
B、随着反应的进行,正反应速率越快,生成氢气的产率将逐渐增大,△t1=△t2时,H2的产率:a~b段小于b~c段,故B正确;
C、从a到c正反应速率增大,之后正反应速率减小,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,说明该反应为放热反应,故C错误;
D、化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,故D错误;
故选:B.
点评:本题考查化学平衡的影响因素分析判断,结合图象分析题意是解题关键,题目难度中等.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1mol石膏(CaSO4?2H2O)加热到150℃,失去大部分结晶水变成熟石膏(2CaSO4?H2O),在此过程中失去结晶水的物质的量为( )
| A、2mol |
| B、1.5mol |
| C、1mol |
| D、0.5mol |
室温下,下列溶液等体积混和,所得溶液pH的一定大于7的是( )
| A、0.1mol?l-1盐酸溶液和0.1mol?l-1氢氧化钠溶液 |
| B、0.1mol?l-1盐酸溶液和0.1mol?l-1氢氧化钡溶液 |
| C、pH=4醋酸溶液和pH=10氢氧化钠溶液 |
| D、pH=4盐酸溶液和pH=10氢氧化钡溶液 |
3mol SO32-恰好将1mol RO4-还原,SO32-被氧化为SO42-.则RO4-在产物中将转化成( )
| A、R2+ |
| B、R+ |
| C、R3+ |
| D、R4+ |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质是一种重要的半导体材料.下列说法中,正确的是( )
| A、X、Y、Z、W的原子半径和原子序数都依次增大 |
| B、W、Z、M元素的气态氢化物热稳定性依次增强 |
| C、M分别和Y、Z所形成化合物都可以和碱反应 |
| D、X分别和M、W所形成的化合物含化学键类型一定相同 |
下列推断合理的是【已知Ag2CrO4和AgCl的Ksp分别是1.12×10-12、1.77×10-10】( )
| A、在高温下,Na2CO3+SiO2=Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3 |
| B、物质的量浓度相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,c(NH4+)的浓度由大到小顺序为:c[(NH4)2SO4]>c[(NH4)2CO3]>c[(NH4)2Fe(SO4)2] |
| C、向1L 0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中c(HCO3-)+c(CO32-)+c(H2CO3)=0.2 mol/L |
| D、T℃时,饱和Ag2CrO4溶液中的c(Ag+)小于饱和AgCl溶液中的c(Ag+) |
3.6g碳在一定量的氧气中燃烧,反应后生成CO和CO2混合气体的平均摩尔质量是32g/mol.则生成的CO的质量是( )
| A、3.3g | B、6.3g |
| C、8.4g | D、13.2g |
