题目内容
9.以下物质间的转化通过一步反应不能实现的是( )| A. | HCl→Cl2→HClO→NaClO | B. | Na→Na2O2→Na2CO3→NaHCO3 | ||
| C. | Al→NaAlO2→Al(OH)3→Al2O3 | D. | Si→SiO2→H2SiO3→Na2SiO3 |
分析 A.二氧化锰与浓盐酸反应生成氯气,氯气与水反应生成HClO,HClO与NaOH反应生成NaClO;
B.Na与氧气反应生成过氧化钠啊,过氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与水、二氧化碳反应生成碳酸氢钠;
C.Al与NaOH反应生成偏铝酸钠,偏铝酸钠与二氧化碳反应生成氢氧化铝,氢氧化铝加热生成氧化铝;
D.二氧化硅不溶于水.
解答 解:A.HCl$\stackrel{MnO_{2}}{→}$Cl2$\stackrel{H_{2}O}{→}$HClO$\stackrel{NaOH}{→}$NaClO,可实现转化,故A不选;
B.Na$\stackrel{O_{2}}{→}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3$\stackrel{CO_{2}、H_{2}O}{→}$NaHCO3,可实现转化,故B不选;
C.Al$\stackrel{NaOH溶液}{→}$NaAlO2$\stackrel{CO_{2}、H_{2}O}{→}$Al(OH)3$\stackrel{△}{→}$Al2O3,可实现转化,故C不选;
D.SiO2→H2SiO3不能一步实现转化,故D选;
故选D.
点评 本题考查物质的性质及转化,为高频考点,把握物质的性质、发生的反应、相互转化为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
19.A,B,C,D,E,F,G为7种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下,其中:B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C与F可形成D和G分子.
(1)A粒子的结构示意图是 .
.
(2)用电子式表示D的形成过程:
(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为NaOH>Mg(OH)2(用化学式表示).
(4)D与G反应的化学方程式是NH3+H2O═NH3•H2O.
(5)C粒子是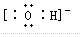 ,F粒子是
,F粒子是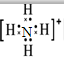 (用电子式表示).
(用电子式表示).
| 微粒 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
 .
.(2)用电子式表示D的形成过程:

(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为NaOH>Mg(OH)2(用化学式表示).
(4)D与G反应的化学方程式是NH3+H2O═NH3•H2O.
(5)C粒子是
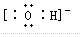 ,F粒子是
,F粒子是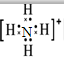 (用电子式表示).
(用电子式表示).
20.A、B、C、X、Y、Z是元素周期表中的前20号元素,且原子序数依次增大.已知它们的部分化合物的性质如下:
回答下列问题:
(1)写出对应元素的名称:A碳、B氮、C氟、X铝、Y硅、Z氯
(2)X、Y、Z三种元素原子半径由大到小的顺序是(用元素符号和“>”表示):Ca>Al>Si
(3)写出B的氢化物与C的氢化物反应后生成物的电子式: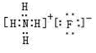 .
.
(4)已知C的单质能在水中产生一种常见的氧化性单质,试写出该反应的化学方程式:2F2+2H2O=4HF+O2.
(5)试比较A和Y的最高价氧化物熔点的高低(用具体物质化学式和“>“、“<“或“=“表示:)CO2<SiO2并说明理由CO2为分子晶体,由分子间作用力结合;而SiO2为原子晶体,由共价键结合,共价键强度大于分子间作用力,故SiO2熔点比CO2的熔点高.
| A的 氢化物 | B的 氢化物 | C的 氢化物 | X的 氧化物 | Y的氢化物 分子构型 | Z原子 |
| 含氢量最高 的有机物 | 水溶液 呈碱性 | 水溶液 呈酸性 | 两性 氧化物 | 正四面体 | 价电子排布为4s2 |
(1)写出对应元素的名称:A碳、B氮、C氟、X铝、Y硅、Z氯
(2)X、Y、Z三种元素原子半径由大到小的顺序是(用元素符号和“>”表示):Ca>Al>Si
(3)写出B的氢化物与C的氢化物反应后生成物的电子式:
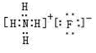 .
.(4)已知C的单质能在水中产生一种常见的氧化性单质,试写出该反应的化学方程式:2F2+2H2O=4HF+O2.
(5)试比较A和Y的最高价氧化物熔点的高低(用具体物质化学式和“>“、“<“或“=“表示:)CO2<SiO2并说明理由CO2为分子晶体,由分子间作用力结合;而SiO2为原子晶体,由共价键结合,共价键强度大于分子间作用力,故SiO2熔点比CO2的熔点高.
4.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 42gC3H6中含有的共用电子对数目为8NA | |
| B. | 标准状况下,22.4L氯气与56g铁充分反应,转移的电子数为3NA | |
| C. | 由6gCaCO3和5gKHCO3组成的混合物中含有的碳原子数为0.1lNA | |
| D. | 1L0.01mol/LKAl(SO4)2溶液中含有的阳离子数为0.02NA |
14.下列关于有机化合物的叙述正确的是( )
| A. | 分子式为C3H6Cl2的有机物有4种同分异构体 | |
| B. | 包装用材料聚氯乙烯分子中含有碳碳双键 | |
| C. | 苯与液溴混合后加入铁粉发生了加成反应 | |
| D. | 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应 |
1.下列关于有机化合物的说法正确的是 ( )
| A. | 2-甲基丁烷的一溴代物有4种 | |
| B. | 乙烯和聚氯乙烯都能使溴水褪色 | |
| C. | 乙醇、乙酸既可用NaOH区分,也可以用小苏打区分 | |
| D. | 乙酸乙酯既能发生加成反应又能发生水解反应 |
13.下列过程需要通电才能进行的是( )
①电离 ②电解 ③电镀 ④电泳 ⑤电化学腐蚀.
①电离 ②电解 ③电镀 ④电泳 ⑤电化学腐蚀.
| A. | ①②③ | B. | ②③⑤ | C. | ②③④ | D. | 全部 |
14.针对实验室制取氨气,下列说法错误的是( )
| A. | 发生装置与用KClO3制取O2的装置相同 | |
| B. | 可用浓硫酸干燥氨气 | |
| C. | 可用向下排空气法收集氨气 | |
| D. | 氨气的验满可以用蘸有浓盐酸的玻璃棒放于试管口附近 |