题目内容
(2012?北京)用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:4HCl+O2
2Cl2+2H2O
(1)已知:i.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
(2)ii.
①H2O的电子式是
 .
.
②反应A的热化学方程式是
③断开1mol H-O 键与断开1mol H-Cl 键所需能量相差约为
(2)对于反应A,如图是4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线.

①曲线b对应的投料比是
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是
| CuO/CuCl3 | 400℃ |
(1)已知:i.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
(2)ii.

①H2O的电子式是


②反应A的热化学方程式是
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
 2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
. 2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol③断开1mol H-O 键与断开1mol H-Cl 键所需能量相差约为
32
32
kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)强
强
.(2)对于反应A,如图是4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线.

①曲线b对应的投料比是
4:1
4:1
.②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是
投料比越高,对应的反应温度越低
投料比越高,对应的反应温度越低
.③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是
30.8%
30.8%
.分析:(1)①水是共价化合物依据电子式书写方法写出电子式;
②反应A中,4mol HCl被氧化,放出115.6kJ的热量,依据热化学方程式书写方法,标注物质聚集状态和对应焓变写出;
③依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,焓变=反应物断键吸收热量-生成物形成化学键放出热量计算;
(2)①在其他条件不变时,O2的量越大,HCl的转化率越大;
②由图可知,当HCl的转化率相同时,温度由低到高对应的投料比为4:1、2:1、1:1,由此可确定温度与投料比的关系;
③依据化学平衡三段式列式计算得到.
②反应A中,4mol HCl被氧化,放出115.6kJ的热量,依据热化学方程式书写方法,标注物质聚集状态和对应焓变写出;
③依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,焓变=反应物断键吸收热量-生成物形成化学键放出热量计算;
(2)①在其他条件不变时,O2的量越大,HCl的转化率越大;
②由图可知,当HCl的转化率相同时,温度由低到高对应的投料比为4:1、2:1、1:1,由此可确定温度与投料比的关系;
③依据化学平衡三段式列式计算得到.
解答:解:(1)①水是共价化合物,氧原子和两个氢原子形成两个共价键,电子式为: ,故答案为:
,故答案为: ;
;
②依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应的热化学方程式为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol;
故答案为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
③焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
4×H-Cl+498-(243×2+4×H-O)=-115.6,得到4×H-O-4×H-Cl=498-486+115.6=127.6
H-O-HCl=31.9≈32,H2O中H-O键比HCl中H-Cl键强,
故答案为:32;强;
(2)①在其他条件不变时,O2的量越大,HCl的转化率越大,由此可确定a为6:1,b为4:1,c为2:1,d为1:1,故答案为:4:1;
②由图可知,当HCl的转化率相同时,温度由低到高对应的投料比为4:1、2:1、1:1,由此可确定温度与投料比的关系是:投料比越高达到相同转化率所需的温度越低,故答案为:投料比越高,对应的反应温度越低;
③由图可读出投料比为2:1、温度为400℃时,HCl的转化率为80%,设投入的HCl为2 mol,O2为1 mol,由此可建立三段式:
4HCl+O2=2Cl2+2H2O
n(起始)/mol 2 1 0 0
n(转化)/mol 1.6 0.4 0.8 0.8
n(平恒)/mol 0.4 0.6 0.8 0.8
所以平衡混合气中Cl2的物质的量分数=
×100%=30.8%.
 ,故答案为:
,故答案为: ;
;②依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应的热化学方程式为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol;
故答案为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
③焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
4×H-Cl+498-(243×2+4×H-O)=-115.6,得到4×H-O-4×H-Cl=498-486+115.6=127.6
H-O-HCl=31.9≈32,H2O中H-O键比HCl中H-Cl键强,
故答案为:32;强;
(2)①在其他条件不变时,O2的量越大,HCl的转化率越大,由此可确定a为6:1,b为4:1,c为2:1,d为1:1,故答案为:4:1;
②由图可知,当HCl的转化率相同时,温度由低到高对应的投料比为4:1、2:1、1:1,由此可确定温度与投料比的关系是:投料比越高达到相同转化率所需的温度越低,故答案为:投料比越高,对应的反应温度越低;
③由图可读出投料比为2:1、温度为400℃时,HCl的转化率为80%,设投入的HCl为2 mol,O2为1 mol,由此可建立三段式:
4HCl+O2=2Cl2+2H2O
n(起始)/mol 2 1 0 0
n(转化)/mol 1.6 0.4 0.8 0.8
n(平恒)/mol 0.4 0.6 0.8 0.8
所以平衡混合气中Cl2的物质的量分数=
| 0.8mol |
| 0.4mol+0.6mol+0.8mol+0.8mol |
点评:本题考查热化学方程式、热化学方程式书写,化学键键能和焓变关系计算,图象分析判断、化学反应转化率计算,题目难度中等.

练习册系列答案
相关题目
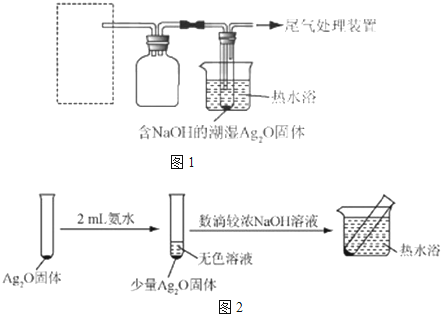
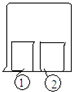 (2012?北京)用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
(2012?北京)用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )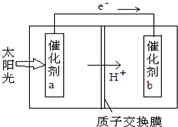 (2012?北京)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
(2012?北京)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )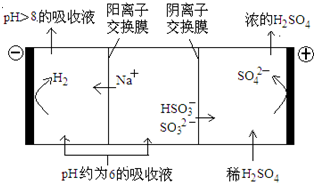 (2012?北京)直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(2012?北京)直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.