题目内容
X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述中不正确的是( )
| A、原子序数和原子半径大小顺序均为:X<Y<Z |
| B、元素X与元素Y能形成离子化合物 |
| C、元素Z最高价氧化物对应水化物具有两性 |
| D、元素Y形成的气态氢化物水溶液呈强酸性 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,X为Na元素,Y的电负性在同周期中最大,Y为Cl元素,Z的离子半径在同周期中最小,Z为Al元素,据此结合元素周期律与物质的性质解答.
解答:
解:X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,X为Na元素,Y的电负性在同周期中最大,Y为Cl元素,Z的离子半径在同周期中最小,Z为Al元素,
A、原子序数Na<Al<Cl,同周期随原子序数增大,原子半径减小,原子半径Na>Al>Cl,故A错误;
B、X为Na元素,Y为Cl元素,二者形成的化合物是氯化钠,属于离子化合物,故B正确;
C、Z为Al元素,其最高价氧化物对应水化物羧基氢氧化铝,氢氧化铝是两性氢氧化物,既能与强酸反应,又能与强碱反应,故C正确;
D、Y为Cl元素,其气态氢化物是HCl,极易溶于是,溶于水呈强酸性,故D正确;
故选A.
A、原子序数Na<Al<Cl,同周期随原子序数增大,原子半径减小,原子半径Na>Al>Cl,故A错误;
B、X为Na元素,Y为Cl元素,二者形成的化合物是氯化钠,属于离子化合物,故B正确;
C、Z为Al元素,其最高价氧化物对应水化物羧基氢氧化铝,氢氧化铝是两性氢氧化物,既能与强酸反应,又能与强碱反应,故C正确;
D、Y为Cl元素,其气态氢化物是HCl,极易溶于是,溶于水呈强酸性,故D正确;
故选A.
点评:本题考查结构性质位置关系,难度不大,注意掌握同周期第一电离能、电负性的变化规律.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
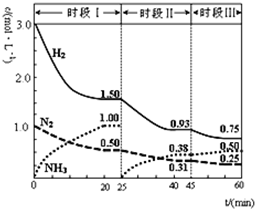 N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.恒容时,体系中各物质浓度随时间变化的曲线如图示.下列说法正确的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.恒容时,体系中各物质浓度随时间变化的曲线如图示.下列说法正确的是( )| A、前20分钟反应内放出的热量为46.2kJ |
| B、第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C、若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是增大压强 |
| D、时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
根据等电子原理,等电子体之间结构相似、物理性质也相近.以下各组粒子不能互称为等电子体的是( )
| A、CO和N2 |
| B、O3和SO2 |
| C、CO2和N2O |
| D、N2H4 和C2H4 |
下列说法中,不正确的是( )
| A、硅单质常用于制造太阳能电池和光纤 |
| B、石灰石在工业上常用制造水泥和玻璃 |
| C、碳酸氢钠在医疗上可用于治疗胃酸过多 |
| D、氧化铝可用于制造耐高温的容器 |
下列事实得出的结论正确的是( )
| A、某雨水样品放置一段时间,pH由5.6变为4.3,说明水中溶解了更多的CO2 |
| B、用一束强光照射经过煮沸的三氯化铁溶液有光的通路,说明已生成氢氧化铁胶体 |
| C、常温下铜可溶于浓硝酸,铁不溶于浓硝酸,说明铜比铁更活泼 |
| D、二氧化硫溶于水所得的溶液可导电,说明二氧化硫是电解质 |
根据碘与氢气反应的热化学方程式下列判断正确的是( )
(i) I2(g)+H2(g) 2HI(g)△H=-9.48kJ/mol
(ii) I2(S)+H2(g)2HI(g)△H=+26.48kJ.
(i) I2(g)+H2(g) 2HI(g)△H=-9.48kJ/mol
(ii) I2(S)+H2(g)2HI(g)△H=+26.48kJ.
| A、1 mol I2(g)中通入2gH2(g),反应放热9.48 kJ |
| B、1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C、反应(i)的产物比反应(ii)的产物稳定 |
| D、反应(ii)的反应物总能量比反应(i)的反应物总能量低 |