题目内容
在10mL0.1mol/L 的醋酸中逐滴加入0.1mol/L 的氢氧化钠溶液,当滴至混合液恰好呈中性时,消耗氢氧化钠溶液的体积( )
| A、等于10mL |
| B、小于10mL |
| C、大于10mL |
| D、无法判断 |
考点:化学方程式的有关计算
专题:
分析:两者等体积恰好完全反应,生成醋酸钠强碱弱酸盐,水解溶液呈碱性,要使溶液呈中性反应碱要小于10ml,由此解答.
解答:
解:两者等体积恰好完全反应,生成醋酸钠强碱弱酸盐,水解溶液呈碱性,要使溶液呈中性反应碱要小于10ml,故选:B.
点评:本题考查酸碱的中和溶液酸碱性,可以让两者恰好完全反应得到溶液的酸碱性,然后分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
杀虫剂“阿乐丹”的结构如图,关于该有机物的说法,正确的是( )


| A、可溶于水 |
| B、能发生银镜反应 |
| C、能与溴水反应 |
| D、能与NaOH溶液发生反应 |
下列说法正确的是( )
| A、一定温度下,反应MgCl2(s)═Mg(s)+Cl2(g)的△H<0△S>0 |
| B、氨气分解反应 2NH3?N2+3H2 达到平衡后,升高温度平衡逆向移动 |
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| D、对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
下列有关说法正确的是( )
| A、相同类型的离子晶体,晶格能越大,形成的晶体越稳定 |
| B、中心原子的杂化方式取决于其配位原子的数目 |
| C、用金属的电子气理论能合理的解释金属易腐蚀的原因 |
| D、H3O+、NH4Cl和[Ag(NH3)2]+中均存在配位键 |
下列有关说法正确的是( )
| A、在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 |
| B、常温下,pH均为5的盐酸、氯化铵溶液中,水的电离程度相同 |
| C、8NH3(g)+6NO(g)═7N2(g)+12H2O(g)△H<0,则该反应一定能自发进行 |
| D、对于乙酸乙酯的水解反应(△H>0),加入少量氢氧化钠溶液并加热,该反应的反应速率和平衡常数均增大 |
形成原电池的条件一般有:①电解质溶液②两个电极③能自发地发生氧化还原反应④形成闭合回路
请根据上述条件判断下列装置中属于原电池的是( )
请根据上述条件判断下列装置中属于原电池的是( )
A、 NaCl溶液 |
B、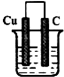 HCl溶液 |
C、 CuSO4溶液 |
D、 蔗糖溶液 |
关于晶体的叙述正确的是( )
| A、原子晶体中,共价键的键能越大,熔、沸点越高 |
| B、分子晶体中,共价键的键能越大,熔、沸点越高 |
| C、存在自由电子的晶体一定是金属晶体,存在阳离子的晶体一定是离子晶体 |
| D、离子晶体中可能存在共价键,分子晶体中可能存在离子键 |