题目内容
9.下列说法正确的是( )| A. | 实验室制取乙酸乙酯时,往大试管中依次加入浓硫酸、无水乙醇、冰醋酸 | |
| B. | 检验C2H5Cl中含Cl元素时,将C2H5Cl和NaOH溶液混合加热后,加硫酸酸化,再滴入硝酸银溶液 | |
| C. | 银氨溶液的配制:向洁净的试管里加入1mL2%的稀氨水,边振荡边滴加2%的AgNO3 溶液 | |
| D. | 实验室制得的粗溴苯通常呈黄色,是因为溶解了少量的Br2 |
分析 A.加入酸液时应避免酸液飞溅;
B.加入硫酸,可生成硫酸银;
C.加入试剂顺序错误;
D.溴易溶于溴苯,溴苯为无色.
解答 解:A.加入酸液时应避免酸液飞溅,应先加入乙醇,再加浓硫酸,防止浓硫酸溶解放热造成液体飞溅,最后慢慢加入冰醋酸,故A错误;
B.加入硫酸,可生成硫酸银,干扰实验现象,应加入硝酸酸化,故B错误;
C.加入试剂顺序错误,应在硝酸银溶液中滴加氨水至程度恰好溶解,故C错误;
D.溴易溶于溴苯,溴苯为无色,粗溴苯通常呈黄色,是因为溶解了少量的Br2,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生分析和实验能力的考查,本题注意把握物质的组成、结构特点,注意实验的严密性和可行性的评价,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.质量分数为25%的氨水的密度是0.92g/cm3,质量分数为5%的氨水的密度是0.98g/cm3,将这两种氨水等体积混合,混合后所得氨水的质量分数( )
| A. | 等于15% | B. | 大于15% | C. | 小于15% | D. | 无法判断 |
17.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一,对下列实验事实的解释正确的是( )
| 现象 | 解释 | |
| A | 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有Na+,一定无K+ |
| B | SO2使酸性高锰酸钾溶液褪色 | SO2具有漂白性 |
| C | 某溶液中先加入稀盐酸无现象,再加入氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 铁加入稀硝酸中有气泡产生 | 铁与稀硝酸发生了置换反应 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验操作或装置能达到实验目的是( )
| A. |  量取109.3mL稀盐酸 | B. |  称量25g烧碱固体 | ||
| C. |  碳酸氢钠受热分解 | D. | 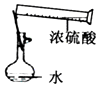 配制一定物质的量浓度的稀硫酸 |
14.下列说法不正确的是( )
| A. | 用烧杯可以精确配制0.1mol/L的NaOH溶液 | |
| B. | 用淀粉溶液检验某溶液中是否存在碘单质 | |
| C. | 可利用丁达尔效应区分胶体与溶液 | |
| D. | 用苯可以萃取溴水中的溴单质 |
1.下列离子方程式书写正确的是( )
| A. | Na与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | FeCl3腐蚀电路板:Fe3++Cu═Fe2++Cu2+ | |
| C. | 向Mg(OH)2中加入盐酸:OH-+H+═H2O | |
| D. | Cl2与水反应:Cl2+H2O═2H++Cl-+ClO- |
18.如图1为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨.用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀.下列说法正确的是( )

| A. | A处通入的气体为CH4,电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| B. | 图2中电解AlCl3溶液的总反应为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 图1中电解质溶液的pH增大 | |
| D. | 电解池中Cl-向x极移动 |
19.下列关于有机物的说法正确的是( )
| A. | 甲烷与氯气发生取代反应,只能生成一氯甲烷 | |
| B. | 乙醇和乙酸都可以与钠反应生成氢气 | |
| C. | 苯和乙烯均能与溴水发生加成反应使溴水褪色 | |
| D. | 甲醛易溶于水,其水溶液具有杀菌消毒作用,可用于浸泡海鲜食品 |