题目内容
5.4g金属铝投入到足量的NaOH水溶液中,则还原产物有( )
| A、0.2mol |
| B、0.3mol |
| C、0.4mol |
| D、0.5mol |
考点:铝的化学性质,化学方程式的有关计算
专题:计算题
分析:金属铝投入到足量的NaOH水溶液中,反应生成偏铝酸钠和氢气,离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,还原产物是氢气,据方程式进行计算即可.
解答:
解:金属铝投入到足量的NaOH水溶液中,反应生成偏铝酸钠和氢气,离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,5.4g金属铝物质的量是
=0.2mol,生成氢气地还原产物,物质的量为0.3mol.
故选B.
| 5.4g |
| 27g/mol |
故选B.
点评:本题考查学生金属铝的化学性质,注意反应方程式的理解是关键,难度不大.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、任何放热的反应在常温条件下一定能发生反应 |
| C、吸热反应只能在加热的条件下才能进行 |
| D、反应是放热还是吸热是由反应物和生成物所具有的总能量所决定的 |
硒是人体中14种必需的营养元素之一,被誉为“生命的奇效元素”,下列关于硒的叙述中错误的是( )
| A、硒的原子半径比氧原子大 |
| B、H2Se沸点比H2O高 |
| C、硒的非金属性比氧元素弱 |
| D、硒的最高价氧化物对应水化物的化学式为H2SeO4 |
在一个固定体积的密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(g)?3C(g)十D(s),达到平衡时C的浓度为1.2mol/L.若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol/L的是( )
| A、4 mol A+2 mol B |
| B、3 mol C+1 mol D+l mol B |
| C、3 mol C+0.8 molD |
| D、1.6 mol A+0.8 mol B+0.6 mol C+0.2 mol D |
下列物质混合时能发生反应,但无明显现象的是( )
| A、二氧化碳与苯酚钠溶液 |
| B、乙酸钠溶液与硫酸氢钠溶液 |
| C、苯酚溶液与氯化铁溶液 |
| D、氢氧化铜悬浊液与甲酸溶液 |
将3mol A和1mol B混合于一体积可变的密闭容器P中,以此时的温度、压强和体积作为起始条件,发生了如下反应:3A(g)+B(g)?2C(g)+D(g),达到平衡时C的浓度为w mol/L保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为w mol/L的是( )
| A、6molA+2molB |
| B、3molA+1molB+2molC |
| C、2molC+1molB+1molD |
| D、1molC+2molD |
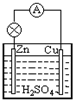 如图,在锌、铜和稀硫酸组成的原电池中,下列说法中正确的是( )
如图,在锌、铜和稀硫酸组成的原电池中,下列说法中正确的是( )| A、铜是正极 |
| B、铜电极的质量减轻 |
| C、锌电极的反应为:2H++2e-=H2↑ |
| D、锌片上发生还原反应 |
有9种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧乙醇⑨苯酚.其中既不能与溴水反应而褪色,也不能使酸性KMnO4溶液褪色的是( )
| A、①②③⑤ | B、④⑥⑦⑧ |
| C、①④⑥⑦ | D、②③⑤⑧⑨ |
某同学用洗涤过,并已检查不漏水的滴定管进行如下操作:①往滴定管内注入标准液;②用标准液润洗滴定管;③滴定;④滴加指示剂于待测液中.正确的操作顺序是( )
| A、①②③④ | B、③①②④ |
| C、④①②③ | D、②①④③ |