题目内容
已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化 反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2,在温度973K和1173K情况下,K1、K2的值分别如下:
请填空:
(1)通过表格中的数值可以推断:反应①是 (填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3= .
(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式 ,据此关系式及上表数据,也能推断出反应③是 (填“吸热”或“放热”)反应.
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有 (填写字母序号,下同).
A.增大压强 B.体积不变时充入稀有气体 C.升高温度
D.使用合适的催化剂 E.在体系中投入少量P2O5固体
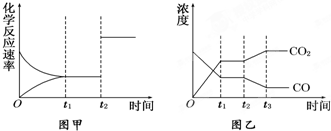
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是 .
②图乙中t2时刻发生改变的条件可能是 .
A.升高温度 B.降低温度 C.加入催化剂 D.增大压强 E.减小压强 F.充入CO2 G.分离出部分CO.
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有
A.增大压强 B.体积不变时充入稀有气体 C.升高温度
D.使用合适的催化剂 E.在体系中投入少量P2O5固体
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是
②图乙中t2时刻发生改变的条件可能是
A.升高温度 B.降低温度 C.加入催化剂 D.增大压强 E.减小压强 F.充入CO2 G.分离出部分CO.

分析:(1)根据温度升高平衡常数的变化判断;
(2)化学平衡常数K=
;
(3)根据盖斯定律,反应①-反应②=反应③,推出k3=
,根据图表可知温度越高K1越大,K2越小,结合K3与K1、K2的关系,推导出温度对K3的影响,再结合平衡移动判断分析;
(4)该反应是一个反应前后气体体积不变的化学反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可以采用升高温度或增大反应物浓度或减小生成物浓度的方法;
(5)图甲中t2时刻改变条件,正逆反应速率都增大但平衡不移动;
图乙中t2时刻改变条件,平衡向逆反应方向移动.
(2)化学平衡常数K=
| K(CO).C(H2O) |
| C(CO2).C(H2) |
(3)根据盖斯定律,反应①-反应②=反应③,推出k3=
| K1 |
| K2 |
(4)该反应是一个反应前后气体体积不变的化学反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可以采用升高温度或增大反应物浓度或减小生成物浓度的方法;
(5)图甲中t2时刻改变条件,正逆反应速率都增大但平衡不移动;
图乙中t2时刻改变条件,平衡向逆反应方向移动.
解答:解:(1)由表中数据可知,温度升高,①的平衡常数增大,说明平衡向正反应方向移动,则正反应吸热,故答案为:吸热;
(2)化学平衡常数K=
,故答案为:
;
(3)根据盖斯定律,反应①-反应②=反应③,所以k3=
,由图表可知,温度升高K1增大,k2减小,所以k3增大,即温度升高,平衡向正反应方向移动,升高温度平衡吸热方向移动,反应③为吸热反应,故答案为:
;吸热;
(4)该反应是一个反应前后气体体积不变的吸热反应,压强、催化剂对化学平衡移动无影响,增大反应物浓度或减小生成物的浓度、升高温度都能使平衡向正反应方向移动,P2O5固体能和水反应生成磷酸,从而减少生成物浓度,平衡向右移动,故选CE;
(5)该反应是一个反应前后气体体积不变的吸热反应,图甲中t2时刻改变条件,正逆反应速率都增大但平衡不移动,改变的条件为增大压强或加入催化剂,图乙中t2时刻改变条件,平衡向逆反应方向移动,二氧化碳浓度增大,一氧化碳浓度减小,可以采用降低温度或增大水蒸气的浓度或减小氢气的浓度,
故选:CD;A.
(2)化学平衡常数K=
| K(CO).C(H2O) |
| C(CO2).C(H2) |
| K(CO).C(H2O) |
| C(CO2).C(H2) |
(3)根据盖斯定律,反应①-反应②=反应③,所以k3=
| K1 |
| K2 |
| K1 |
| K2 |
(4)该反应是一个反应前后气体体积不变的吸热反应,压强、催化剂对化学平衡移动无影响,增大反应物浓度或减小生成物的浓度、升高温度都能使平衡向正反应方向移动,P2O5固体能和水反应生成磷酸,从而减少生成物浓度,平衡向右移动,故选CE;
(5)该反应是一个反应前后气体体积不变的吸热反应,图甲中t2时刻改变条件,正逆反应速率都增大但平衡不移动,改变的条件为增大压强或加入催化剂,图乙中t2时刻改变条件,平衡向逆反应方向移动,二氧化碳浓度增大,一氧化碳浓度减小,可以采用降低温度或增大水蒸气的浓度或减小氢气的浓度,
故选:CD;A.
点评:本题考查化学平衡移动问题,题目难度较大,本题注意盖斯定律的运用,理解平衡常数的意义,注意反应③是一个反应前后气体体积不变的可逆反应,压强和催化剂对其平衡无影响.

练习册系列答案
相关题目
 2NH3是工业上合成氨的重要反应.
2NH3是工业上合成氨的重要反应.
 2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol
2NH3(g)△H=2(E1-E3)或-2(E3-E1)kg/mol