题目内容
13.下列溶液中粒子的物质的量浓度关系正确的是( )| A. | pH相同的①NH4C1、②NH4Al(SO4)2、③NH4HSO4三种溶液的c(NH4+):①<②<③ | |
| B. | 20mL 0.1 mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c( H+) | |
| C. | 0.1mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| D. | 常温下,pH=7的NH4C1与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
分析 A.硫酸氢铵在溶液中完全电离出氢离子,其浓度最小;铝离子水解溶液呈酸性,则NH4Al(SO4)2的浓度小于氯化铵;
B.反应后溶质为等浓度的醋酸钠、醋酸、NaCl,溶液呈酸性,则c(H+)>c(OH-),说明醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COO-)>c(CH3COOH),结合物料守恒分析;
C.反应后溶质为碳酸钠,碳酸根离子水解生成碳酸氢根离子和氢氧根离子,由于氢氧根离子还来自水的电离,则c(OH-)>c(HCO3-);
D.溶液呈中性,则c(H+)=c(OH-),结合电荷守恒判断.
解答 解:A.pH相同的①NH4C1、②NH4Al(SO4)2、③NH4HSO4三种溶液,③中能够电离出氢离子,其浓度最小,③的溶液中c(NH4+)最小;①中只有铵根离子水解,而②中铝离子也水解,则①中铵根离子浓度大于②,所以pH相同时三种溶液中c(NH4+)大小为:①>②>③,故A错误;
B.20mL 0.1 mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后呈酸性,则c(H+)>c(OH-),说明醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COO-)>c(CH3COOH),根据物料守恒可知:c(CH3COO-)>c(Cl-)>c(CH3COOH),所得溶液中离子浓度大小为:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c( H+),故B正确;
C.0.1mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,反应后溶质为碳酸钠,由于氢氧根离子还来自水的电离,则c(OH-)>c(HCO3-),正确的离子浓度大小为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-),故C错误;
D.常温下pH=7的NH4C1与氨水的混合溶液呈中性,则c(H+)=c(OH-),根据核电荷数可得:c(Cl-)=c(NH4+),正确的离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)=c(OH-),故D错误;
故选B.
点评 本题考查离子浓度大小比较,题目难度不大,明确反应后溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理的含义,试题有利于提高学生的分析能力及灵活应用能力.

①微粒半径:S2->Cl->F
②氢化物的稳定性:HF>HCl>H2S>H2Te
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>HClO4>H2SeO4
⑥非金属性:F>Cl>S>Se
⑦单质与水反应的剧烈程度:F2<Cl2<Br2<I2.
| A. | ①②④⑥ | B. | ①③④ | C. | ①③ | D. | ⑤⑥ |
| A. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$\stackrel{H_{2}}{→}$Si | |
| B. | FeS2$→_{煅烧}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(g)}{→}$NH4Cl(s) | |
| D. | 由NaCl制漂粉精:NaCl(aq)$\stackrel{点解}{→}$Cl2$\stackrel{澄清石灰水}{→}$漂粉精 |
| A. | F-的结构示意图: | |
| B. | NaCl的电子式: | |
| C. | 8个中子的碳原子的核素符号:${\;}_{6}^{14}$C | |
| D. | CO2的结构式:O=C=O |
| A. | 标准状况下,14g氮气含有的核外电子数为5NA | |
| B. | 32 g S8单质(S8分子结构如图)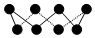 中含有的S-S键个数为8NA 中含有的S-S键个数为8NA | |
| C. | 17g的氢氧根离子中含有的电子数为9NA | |
| D. | 常温下,4.6gNa和足量的O2完全反应失去电子数为0.2NA |
①X被氧化;
②X是氧化剂;
③Y2+既具有氧化性也具有还原性;
④Y2+是氧化产物;
⑤Y3+的氧化性比X2+的氧化性强.
| A. | ①②⑤ | B. | ①③⑤ | C. | ②④⑤ | D. | ③④⑤ |
| A. | 大于9a×10-3mol,小于18a×10-3mol | B. | 都等于9a×10-3mol | ||
| C. | 都等于18a×10-3mol | D. | 都小于9a×10-3mol |
| A. | 盐酸+氢氧化钠溶液 | B. | 氯化钠溶液+硫酸钾溶液 | ||
| C. | 硝酸钙溶液+碳酸钠溶液 | D. | 稀硫酸+碳酸钠溶液 |



