题目内容
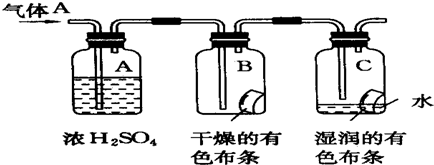
某学生用图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:
(1)该项研究(实验)的主要目的是
(2)浓H2SO4的作用是 .与研究目的直接相关的实验现象是
(3)从物质性质的方面来看,这样的实验设计还存在安全隐患,表现是 .克服安全隐患的措施是(用化学方程式表示): .
(4)若将剩余的氯气收集,测其在标准状况下的体积为11.2升,让其与氢气充分化合,该反应的方程式为 ;将生成的气体溶于水,配成500ml溶液,则该溶液中溶质的物质的量浓度为 .

(1)该项研究(实验)的主要目的是
(2)浓H2SO4的作用是
(3)从物质性质的方面来看,这样的实验设计还存在安全隐患,表现是
(4)若将剩余的氯气收集,测其在标准状况下的体积为11.2升,让其与氢气充分化合,该反应的方程式为
考点:氯气的化学性质
专题:元素及其化合物
分析:(1)本实验的目的是探究氯气具有漂白性的条件下,干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性;
(2)浓硫酸具有吸水性,干燥的氯气不具有漂白性,据此进行解答;
(3)氯气有毒,不能排放在空气中,克服的措施可以用氢氧化钠溶液吸收多余的氯气;
(4)氯气与氢气化合生成氯化氢,然后根据c=
,结合氯守恒分析求解.
(2)浓硫酸具有吸水性,干燥的氯气不具有漂白性,据此进行解答;
(3)氯气有毒,不能排放在空气中,克服的措施可以用氢氧化钠溶液吸收多余的氯气;
(4)氯气与氢气化合生成氯化氢,然后根据c=
| n |
| V |
解答:
解:(1)本实验为对比实验,将氯气分别通入干燥布条和湿润布条,根据实验现象的不同来探究氯气具有漂白性的条件,故答案为:探究氯气具有漂白性的条件;
(2)浓硫酸具有吸水性,常用作干燥剂,在实验中吸收气体A中的水的作用,实验现象是B中的布条不褪色,C中的布条褪色,故答案为:吸收气体A中的水蒸气;B中的布条不褪色,C中的布条褪色;
(3)氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收,发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:没有尾气处理装置,造成环境污染;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)氢气与氯气反应的方程式为:H2+Cl2
2HCl,n(Cl2)=
=0.5mol,所以c=
=2 mol?L-1,
故答案为:H2+Cl2
2HCl;2 mol?L-1.
(2)浓硫酸具有吸水性,常用作干燥剂,在实验中吸收气体A中的水的作用,实验现象是B中的布条不褪色,C中的布条褪色,故答案为:吸收气体A中的水蒸气;B中的布条不褪色,C中的布条褪色;
(3)氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收,发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:没有尾气处理装置,造成环境污染;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)氢气与氯气反应的方程式为:H2+Cl2
| ||
| 11.2L |
| 22.4L/mol |
| 0.5×2 |
| 0.5 |
故答案为:H2+Cl2
| ||
点评:本题考查氯气的性质,氯气没有漂白性,氯水的漂白性是溶液中次氯酸的表现的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
需要加入适当的氧化剂才能实现的反应( )
| A、SO3→HSO4- |
| B、MnO4-→Mn2+ |
| C、PCl3→PCl5 |
| D、CO2→H2CO3 |
反应A(g)+3B(g)?2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
| A、v(A)=0.15 mol?L-1?min-1 |
| B、v(B)=0.015 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(D)=0.45 mol?L-1?min-1 |
下列离子反应方程式,书写正确的是( )
| A、碳酸氢钠溶液中加入醋酸:CO32-+2H+=H2O+CO2↑ |
| B、稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C、碳酸钙中加入盐酸:CO32-+2H+=H2O+CO2↑ |
| D、氢氧化钠溶液中加入硫酸:H++OH-=H2O |
下列物质中属于有机物的是( )
| A、甲醇 | B、苏打 | C、水泥 | D、玻璃 |
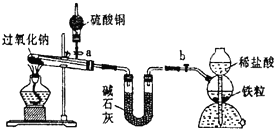 Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与C02、H20反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验.
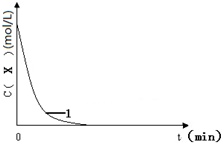 已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.
已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.