题目内容
其它条件不变,增大反应体系的压强,下列数据会明显增大的是( )
| A、二氧化硫与氧气反应生成三氧化硫气体的化学反应速率v |
| B、醋酸的电离度α |
| C、合成氨的化学平衡常数K |
| D、水的离子积常数Kw |
考点:化学平衡常数的含义,离子积常数
专题:化学平衡专题,电离平衡与溶液的pH专题
分析:A、对有气体参加的反应,增大压强化学反应速率加快;
B、电离度α,是温度的函数;
C、化学平衡常数K,是温度的函数;
D、水的离子积常数Kw,是温度的函数.
B、电离度α,是温度的函数;
C、化学平衡常数K,是温度的函数;
D、水的离子积常数Kw,是温度的函数.
解答:
解:A、对有气体参加的反应,增大压强化学反应速率加快,故A正确;
B、电离度α,是温度的函数,压强改变,电离度不变,故B错误;
C、化学平衡常数K,是温度的函数,压强改变,平衡常数不变,故C错误;
D、水的离子积常数Kw,是温度的函数,压强改变,水的离子积常数不变,故D错误;
故选A.
B、电离度α,是温度的函数,压强改变,电离度不变,故B错误;
C、化学平衡常数K,是温度的函数,压强改变,平衡常数不变,故C错误;
D、水的离子积常数Kw,是温度的函数,压强改变,水的离子积常数不变,故D错误;
故选A.
点评:本题考查电离度α、化学平衡常数、水的离子积常数和化学反应速率的影响因素,学生要注意电离度α、化学平衡常数、水的离子积常数是温度的函数,比较容易.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列实验方法:①加热蒸馏95%的洒精,以分离其中的水和乙醇;②用分液法分离H2O和CCl4的混合物;③用升华法分离I2和砂子的混合物;④用过滤法分离MnO2和KCl的混合物;你认为上述方法( )
| A、只有①不正确 |
| B、只有②不正确 |
| C、只有③④正确 |
| D、全部正确 |
下列溶液中的Cl-浓度与50mL 1mol?L-1 BaCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1 mol?L-1 NaCl溶液 |
| B、75 mL 1 mol?L-1 MgCl2溶液 |
| C、150 mL 2 mol?L-1 KClO3溶液 |
| D、75 mL 1 mol?L-1 AlCl3溶液 |
复杂的体系中,研究化学反应的先后顺序有利于解决问题.下列物质或微粒参与反应先后顺序判断正确的是( )
| A、含有等物质的量的[Al(OH)4]-,OH-,CO32-的溶液中逐滴加入盐酸:[Al(OH)4]-,Al(OH)3,OH-,CO32- |
| B、含有等物质的量的FeBr2和Fel2溶液中缓缓通入Cl2:I-,Br-,Fe2+ |
| C、在等物质的量的K2CO3和KOH混合溶液中缓缓通入CO2:K2CO3,KOH |
| D、在含有等物质的量的Fe3+,Cu2+,H+的溶液中逐渐加入锌粉:Fe3+,Cu2+,H+,Fe2+ |
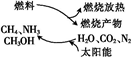 “世界环境日”主题之一是促进物质的循环利用.有专家提出:如果对燃料燃烧产物如CO2、H2O、N2等利用太阳能让它们重新组合,使之能够实现如图转化,在此构想中太阳能最终转化为( )
“世界环境日”主题之一是促进物质的循环利用.有专家提出:如果对燃料燃烧产物如CO2、H2O、N2等利用太阳能让它们重新组合,使之能够实现如图转化,在此构想中太阳能最终转化为( )| A、化学能 | B、热能 |
| C、生物能 | D、电能 |
若硝酸铵受热分解产物是HNO3、N2、H2O,则该反应中被氧化与被还原的氮原子数之比为( )
| A、5:3 | B、5:4 |
| C、1:1 | D、3:5 |
某有机物链状分子中含n个次甲基,m个 亚甲基,a个甲基,其余为羟基.则该有机物分子中羟基的个数为( )
| A、2n+3m-a |
| B、n+m+a |
| C、m+2-a |
| D、m+2n+2-a |
下列各组离子因发生氧化还原反应在水溶液中不能大量共存的是( )
| A、Na+ H+ NO3- HCO3- |
| B、Fe2+ H+ Cl- NO3- |
| C、Fe3+ Ca2+ OH- NO3- |
| D、Ba2+ Na+ OH-NO3- |
在25℃时,对于0.1moL?L-1CH3COONa溶液的说法正确的是( )
A、加水稀释后,溶液中
| ||
| B、加入少量NaOH固体,c(CH3COO-)减小 | ||
| C、该溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||
| D、与0.1mol?L-1硝酸等体积混合后:c(Na+)=c(NO3-)>c(CH3COO-)>c(H+)>c(OH-) |