题目内容
20.化学与社会、生产、生活密切相关.下列说法正确的是( )| A. | 聚氯乙烯可用作制食品包装袋的原料 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 晶体硅可用作制造太阳能电池和光导纤维 | |
| D. | 含硫燃料燃烧产生的二氧化硫是形成酸雨的罪魁祸首 |
分析 A.聚氯乙烯使用时产生有毒物质;
B.从海水中提取NaCl,为晒盐过程,没有新物质生成;
C.光导纤维的成分为二氧化硅;
D.二氧化硫的排放导致酸雨的发生.
解答 解:A.聚氯乙烯使用时产生有毒物质,则聚氯乙烯不能作制食品包装袋的原料,故A错误;
B.从海水中提取NaCl,为晒盐过程,没有新物质生成,为物理变化,而提取溴、Mg、碘等需要发生化学变化,故B错误;
C.光导纤维的成分为二氧化硅,而晶体硅可用作制造太阳能电池,故C错误;
D.二氧化硫的排放导致酸雨的发生,则含硫燃料燃烧产生的二氧化硫是形成酸雨的罪魁祸首,故D正确;
故选D.
点评 本题考查物质的性质、应用,为高频考点,把握物质的性质、化学与生活、性质与用途等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
11.下列选项正确的是( )
| A. | 汽车催化转化器中尾气处理反应的化学方程式为CO+NO$\frac{\underline{\;\;△\;\;}}{\;}$C+NO2 | |
| B. | 铁红溶于足量氢碘酸的离子方程式为Fe2O3+6H+═2Fe3++3H2O | |
| C. | 加入铝粉能产生氢气的溶液中可能存在大量的:K+、Ba2+、AlO2-、Cl- | |
| D. | pH=0的溶液中可能存在大量的:Na+、Fe2+、SO42-、ClO- |
12.某消毒液的主要成分为NaClO,下列有关该混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 | |
| C. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 | |
| D. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O |
9.下列相应叙述正确的是( )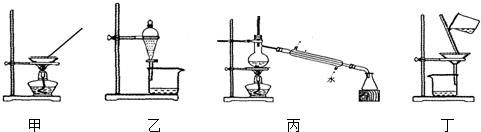

| A. | 可用甲装置蒸发氯化铵溶液制氯化铵 | |
| B. | 可用乙装置加水分离碘酒中的碘 | |
| C. | 可用丙装置分离乙醇和水 | |
| D. | 可用丁装置分离FeCl3溶液和Fe(OH)3胶体 |
16.有关如图四个常用电化学装置的叙述中正确的是( )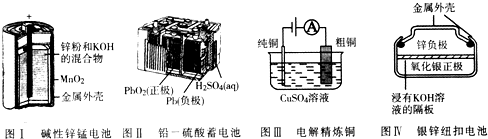

| A. | 图I所示电池中,锌极电极反应为Zn-2e-═Zn2+ | |
| B. | 图Ⅱ所示电池放电过程中,每转移1mo1电子,生成1mol PbSO4 | |
| C. | 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 | |
| D. | 图Ⅳ所示电池中,Ag2O在电池工作过程中被氧化为Ag |
5.下列有关FeCl3溶液的叙述正确的是( )
| A. | 该溶液中,K+、Fe2+、SCN-、Br-可以大量共存 | |
| B. | 与KI溶液反应的离子方程式为Fe3++2I-═Fe2++I2 | |
| C. | 与Na2CO3溶液反应的离子方程式为2Fe3++3CO32-+3H2O═2Fe(OH)3↓+3CO2↑ | |
| D. | 与Mg(OH)2悬浊液反应的离子方程式为3OH-+Fe3+═Fe(OH)3↓ |
10.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色透明的溶液中:Na+、MnO4-、NO3-、Br- | |
| B. | 0.1 mol•L-1CaCl2溶液中:Mg2+、NH4+、CO32-、SO42- | |
| C. | Kw/c(OH-)=10-12 mol•L-1的溶液:Na+、K+、SiO32-、Cl- | |
| D. | 水电离产生的c(H+)=10-12 mol•L-1的溶液中:K+、Fe2+、NO3-、Cl- |
7.下列事实或实验可以表明H2SO3的酸性强于H2CO3的是( )
| A. | 硫的非金属性比碳强 | |
| B. | SO2气体依次通过NaHCO3溶液、澄清石灰水,澄清石灰水变浑浊 | |
| C. | SO2和CO2气体分别通入水中至饱和,测定两溶液的pH,前者小于后者 | |
| D. | 室温下测定均为0.1mol/L的NaHSO3和NaHCO3溶液的pH,前者小于后者 |