题目内容
13.仅改变下列一个条件,通过提高活化分子的百分率来提高反应速率的是( )①加热②加压③加催化剂④加大反应物浓度.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
分析 升高温度、加入催化剂都能提高活化分子百分数,据此分析解答.
解答 解:①加热吸收热量,使部分非活化分子转化为活化分子,从而提高百分数,提高化学反应速率,故正确;
②加压,增大单位体积内活化分子个数,但不增大活化分子百分数,故错误;
③加催化剂,降低反应所需活化能,增大活化分子百分数,从而提高化学反应速率,故正确;
④加大反应物浓度,增大单位体积内活化分子个数,但不增大活化分子百分数,故错误;
故选A.
点评 本题考查化学反应速率影响因素,为高频考点,侧重考查学生对化学反应速率影响因素的理解和掌握,明确改变反应速率原理是解本题关键,题目难度不大.

练习册系列答案
相关题目
3.天然气的主要成分是甲烷,还含有一定量的乙烷、丙烷等可燃性气体.下列有关说法不正确的是( )
| A. | 甲烷与丙烷互为同系物 | |
| B. | 甲烷的一氯代物只有一种结构证明甲烷是正四面体结构而非平面正方形结构 | |
| C. | 甲烷、乙烷、丙烷中的化学键都是极性共价键 | |
| D. | 乙烷和氯气在光照的条件下可发生取代反应,生成多种氯代烃 |
4.胶体分散系与其它分散系的本质差别是( )
| A. | 分散质直径大小 | B. | 分散质粒子是否带电 | ||
| C. | 是否稳定 | D. | 是否有丁达尔现象 |
1.用NA表示阿伏伽德罗常数,下列说法不正确的是( )
| A. | 1.6g 由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | Na2O和Na2O2中阴阳离子个数比都为1:2 | |
| C. | 18g H2O含有10NA个质子 | |
| D. | 标准状况下,11.2L H2O中含有的分子的数目为0.5 NA |
8.下列系统命名法正确的是( )
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,3-二乙基-1-戊烯 | D. | 3,4-二甲基-4-乙基己烷 |
8.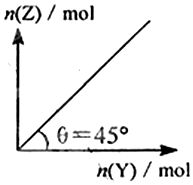 在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
 在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )| A. | 平衡时Y的转化率为$\frac{a}{b}$% | |
| B. | 向容器中再加入少量X,则Y的转化率增大 | |
| C. | 再通入Y,重新达到平衡时W的体积分数不变 | |
| D. | 保持压强一定,当原反应在较高温度下建立平衡时,图中θ<45° |
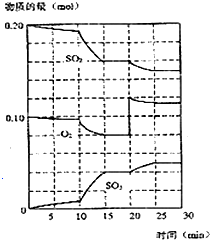 在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1
在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1