题目内容
12.下列反应的离子方程式正确的是( )| A. | 氯化镁溶液中加氨水:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+ | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 稀硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
分析 A.氯化镁溶液与氨水反应生成氢氧化镁沉淀和氯化铵;
B.离子方程式两边正电荷不相等,违反了电荷守恒;
C.氢离子、氢氧根离子的系数不满足硫酸、氢氧化钡的化学式组成;
D.碳酸钙和醋酸都不能拆开,需要保留化学式.
解答 解:A.氯化镁溶液中加氨水,反应生成氢氧化镁沉淀和氯化铵,反应的离子方程式为:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+,故A正确;
B.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.稀硫酸与氢氧化钡溶液混合,反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C错误;
D.醋酸为弱酸,离子方程式中醋酸需要保留分子式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
3.下列物质的性质比较,正确的是( )
| A. | 酸性:H2CO3>HNO3 | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:Si>P | D. | 气态氢化物稳定性:H2O>H2S |
20.锗(Ge)是第4周期ⅣA族元素,处于周期表中金属区与非金属区的交界线上,下列叙述正确的是( )
| A. | 锗是一种金属性很强的元素 | B. | 锗酸(H4GeO4)是难溶于水的强酸 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗的单质具有半导体的性能 |
7.已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平. 现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
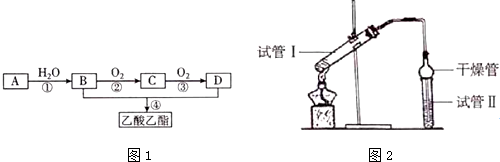
(1)有机物D中官能团的名称为羧基,①、④的反应类型分别为加成反应、酯化反应或取代反应.
(2)反应④的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(3)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图2的装罝制备乙酸乙酯.
①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:防倒吸.
②试管Ⅱ中加入的试剂是饱和Na2CO3溶液,其作用是:吸收乙酸和乙醇,降低乙酸乙酯的溶解度.
③为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用该装置进行了以下4 个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ,再测其中有机层的厚度,实验记录如下:
实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用,则进行实验D时应加入2 mL6mol•L-1的盐酸.分析实验A和实验C的数据,可以推断出浓H2SO4的吸水(填“催化”或“吸水”)作用提高了乙酸乙酯的产率.
(4)乙醇在一定条件下可转化为有机物E,E的相对分子质里为74,其分子中碳、氢的质量分数分别为64.9%、13.5%,其余为氧.求E的化学式C原子个数=$\frac{74×64.9%}{12}$≈4、H原子个数=$\frac{74×13.5%}{1}$≈10,则O原子个数=$\frac{74-12×4-1×10}{16}$=1,则C、H、O原子个数之比=4:10:1,则E的化学式为C4H10O(需写出计算过程).

(1)有机物D中官能团的名称为羧基,①、④的反应类型分别为加成反应、酯化反应或取代反应.
(2)反应④的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(3)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图2的装罝制备乙酸乙酯.
①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:防倒吸.
②试管Ⅱ中加入的试剂是饱和Na2CO3溶液,其作用是:吸收乙酸和乙醇,降低乙酸乙酯的溶解度.
③为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用该装置进行了以下4 个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ,再测其中有机层的厚度,实验记录如下:
| 实验编号 | 试管I中试剂 | 试管Ⅱ中有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、2mL 18mol•L-1浓硫酸 | 3.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL 乙醇、2mL 乙酸 2mL3mol•L-1H2SO4 | 0.6 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 0.6 |
(4)乙醇在一定条件下可转化为有机物E,E的相对分子质里为74,其分子中碳、氢的质量分数分别为64.9%、13.5%,其余为氧.求E的化学式C原子个数=$\frac{74×64.9%}{12}$≈4、H原子个数=$\frac{74×13.5%}{1}$≈10,则O原子个数=$\frac{74-12×4-1×10}{16}$=1,则C、H、O原子个数之比=4:10:1,则E的化学式为C4H10O(需写出计算过程).
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol Fe在0.1mol Cl2中充分燃烧,转移电子数为0.3NA | |
| B. | 用MnO2与浓盐酸制取Cl2时,每生成1 mol Cl2则转移电子数为NA | |
| C. | 1L 0.1mol•L-1(NH4)2SO4溶液中含有NH4+的数目为0.2 NA | |
| D. | 23g钠在足量氧气中充分燃烧,转移电子数为NA |
1.下列关于铝热剂的说法中,错误的是( )
| A. | 铝热剂的反应原理是利用铝的强还原剂 | |
| B. | 铝热剂的反应常用于冶炼难熔金属 | |
| C. | 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以是一个吸热反应 | |
| D. | 铝和所有金属物都可以组成铝热剂 |
14.化学能可与其他形式的能量相互转化.下列反应是由热能转化成化学能的是( )
| A. | CaCO3高温?CaO+CO2↑ | |
| B. | Pb+PbO2+2H2SO4?充电放电2PbSO4+2H2O | |
| C. | 2H2O 电解?2H2↑+O2↑ | |
| D. | 6nH2O+6nCO2→叶绿体光(C6H12O6)n+6nH2O |