题目内容
科学家一直致力于“人工固氮”的方法研究.(1)目前合成氨的技术原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,该反应的能量变化如图所示.
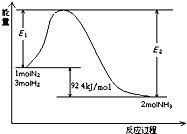
①在反应体系中加入催化剂,反应速率增大,E2的变化是: .(填“增大”、“减小”或“不变”).
②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g)?2NH3(g),5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.氮气的平均反应速率v(N2)= ,H2的转化率为 ,该反应在此温度下的化学平衡常数为 .(后两空保留小数点后一位)
③欲提高②容器中H2的转化率,下列措施可行的是 .
A.向容器中按原比例再充入原料气
B.向容器中再充入惰性气体
C.改变反应的催化剂
D.液化生成物分离出氨
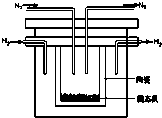
(2)1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传导H+),从而实现了高转化率的电解法合成氨.其实验装置如图所示.阴极的电极反应式为 .
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=akJ/mol
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
此合成反应的a 0.(填“大于”、“小于”或“等于”)

①在反应体系中加入催化剂,反应速率增大,E2的变化是:
②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g)?2NH3(g),5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.氮气的平均反应速率v(N2)=
③欲提高②容器中H2的转化率,下列措施可行的是
A.向容器中按原比例再充入原料气
B.向容器中再充入惰性气体
C.改变反应的催化剂
D.液化生成物分离出氨
(2)1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传导H+),从而实现了高转化率的电解法合成氨.其实验装置如图所示.阴极的电极反应式为

(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=akJ/mol
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
考点:化学平衡的计算,化学平衡的影响因素,电解原理
专题:化学平衡专题
分析:(1)①催化剂降低反应的活化能;
②依据化学平衡的三段式列式计算平衡量;依据化学反应速率和转化率概念计算结果;
③根据影响化学平衡的影响条件分析判断,平衡向正向进行,增大另一种物质的浓度会提高氢气转化率;
(2)电解池的阴极发生得电子的还原反应;
(3)根据温度对化学平衡移动方向的影响来判断反应的吸放热情况.
②依据化学平衡的三段式列式计算平衡量;依据化学反应速率和转化率概念计算结果;
③根据影响化学平衡的影响条件分析判断,平衡向正向进行,增大另一种物质的浓度会提高氢气转化率;
(2)电解池的阴极发生得电子的还原反应;
(3)根据温度对化学平衡移动方向的影响来判断反应的吸放热情况.
解答:
解:(1)①在反应体系中加入催化剂,反应速率增大,降低了反应的活化能,依据图示方向可知E2减小,故答案为:减小;
②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生反应:N2(g)+3H2(g)?2NH3(g)5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.
依据化学平衡的三段式列式计算:起始量=平衡量+变化量
N2(g)+3H2(g)?2NH3(g)
起始量(mmol) 0.3 0.9 0
变化量(mol) 0.1 0.3 0.2
平衡量(mol) 0.2 0.6 0.2
氮气的平均反应速率v(N2)=
=0.01mol/L?min;
H2的转化率=
×100%=33.3%,
K=
=3.7 L2/mol2,
故答案为:0.01mol?L-1?min-1;33.3%;3.7 L2/mol2;
③A、向容器中按原比例再充入原料气,相当于增大容器内的压强,平衡正向进行,提高氢气的转化率,故A正确;
B、向容器中再充入惰性气体,则各组分的浓度不变,平衡不移动,所以反应物的转化率不会改变,故B错误;
C、改变反应的催化剂,不改变化学平衡,不能提高氢气转化率,故C错误;
D、液化生成物分离出氨,减少生成物,平衡正向进行,提高氢气转化率,故D正确;
故选AD;
(2)电解池的阴极发生得电子的还原反应,在合成氨中,氮气得电子,所以阴极反应为N2+6H++6e-=2NH3,故答案为:N2+6H++6e-=2NH3;
(3)温度对化学平衡移动方向的影响是:温度越高,氨气的量越大,所以升高温度,平衡向右进行,反应是吸热反应,故答案为:大于.
②将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生反应:N2(g)+3H2(g)?2NH3(g)5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.
依据化学平衡的三段式列式计算:起始量=平衡量+变化量
N2(g)+3H2(g)?2NH3(g)
起始量(mmol) 0.3 0.9 0
变化量(mol) 0.1 0.3 0.2
平衡量(mol) 0.2 0.6 0.2
氮气的平均反应速率v(N2)=
| ||
| 5min |
H2的转化率=
| 0.3mol |
| 0.9mol |
K=
(
| ||||
|
故答案为:0.01mol?L-1?min-1;33.3%;3.7 L2/mol2;
③A、向容器中按原比例再充入原料气,相当于增大容器内的压强,平衡正向进行,提高氢气的转化率,故A正确;
B、向容器中再充入惰性气体,则各组分的浓度不变,平衡不移动,所以反应物的转化率不会改变,故B错误;
C、改变反应的催化剂,不改变化学平衡,不能提高氢气转化率,故C错误;
D、液化生成物分离出氨,减少生成物,平衡正向进行,提高氢气转化率,故D正确;
故选AD;
(2)电解池的阴极发生得电子的还原反应,在合成氨中,氮气得电子,所以阴极反应为N2+6H++6e-=2NH3,故答案为:N2+6H++6e-=2NH3;
(3)温度对化学平衡移动方向的影响是:温度越高,氨气的量越大,所以升高温度,平衡向右进行,反应是吸热反应,故答案为:大于.
点评:本题考查学有关电化学以及化学平衡的有关计算、化学平衡移动原理等知识,考查角度广,难度大.

练习册系列答案
相关题目
下列各组中的两种物质相互作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是( )
| A、Al和 NaOH溶液 |
| B、NaOH溶液和AlCl3溶液 |
| C、Na和O2 |
| D、NaOH溶液和CO2 |
下列物质属于不属于混合物的是( )
| A、纯碱 | B、石油 | C、煤 | D、碱石灰 |
由于Fe(OH)2极易被氧化,所以实验室里很难用亚铁盐溶液与烧碱反应制的白色纯净的Fe(OH)2沉淀.应用如图所示的电解实验可制得白色纯净Fe(OH)2沉淀,两电极的材料分别为石墨和铁.下列说法正确的是( )
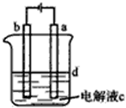

| A、a电极发生的电极反应:4OH--4e-=O2↑+2H2O |
| B、为了在较短时间内看到白色沉淀,可适当加大电压 |
| C、c可以是氯化钠溶液,d可以是苯 |
| D、为了在较短时间内看到白色沉淀,可以剧烈地搅拌溶液 |
 (1)用l体积SO2和3体积空气混合,在450℃以上通过V2O5催化剂,发生如下反应:2SO2(g)+O2(g)?2SO3(g).一段时间后达到平衡,若此时同温同压下测得反应前后混合气体的密度比为0.9:1,则SO2平衡转化率为
(1)用l体积SO2和3体积空气混合,在450℃以上通过V2O5催化剂,发生如下反应:2SO2(g)+O2(g)?2SO3(g).一段时间后达到平衡,若此时同温同压下测得反应前后混合气体的密度比为0.9:1,则SO2平衡转化率为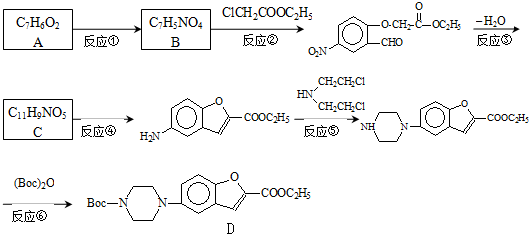
 ;
;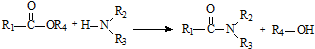 .
. 和
和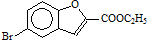 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式