题目内容
5. 用下图装置可以测定混合气体中ClO2的含量
用下图装置可以测定混合气体中ClO2的含量Ⅰ.在锥形瓶中加入足量的碘化钾,用50mL水溶解后,再加入3mL稀硫酸;
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中;
Ⅴ.用0.1000mol•L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-═2I-+S4O62-),指示剂显示终点时共用去20.00mL硫代硫酸钠溶液.在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为2ClO2+10I-+8H+═2Cl-+5I2+4H2O
②玻璃液封装置的作用是吸收残留的ClO2气体(避免碘的逸出)
③V中加入的指示剂通常为淀粉溶液,滴定至终点的现象是溶液由蓝色变为无色,且半分钟内溶液颜色不再改变
④用ClO2处理过的饮用水会含有一定最的亚氯酸盐.若要除去超标的亚氯酸盐,下列物质最适宜的是d(填标号)a.明矾b.碘化钾c.盐酸d.硫酸亚铁.
分析 ①由题目信息可知,ClO2通入锥形瓶与酸性碘化钾溶液反应,氧化I-为I2,自身被还原为Cl-,同时生成水;
②玻璃液封装置可防止有害气体逸出;
③淀粉遇碘单质变蓝;
④亚氯酸盐具有氧化性,Fe2+将ClO2-还原成Cl-,Fe2+ 被氧化为铁离子.
解答 解:①由题目信息可知,ClO2通入锥形瓶与酸性碘化钾溶液反应,氧化I-为I2,自身被还原为Cl-,同时生成水,反应离子方程式为2ClO2+10I-+8H+═2Cl-+5I2+4H2O,
故答案为:2ClO2+10I-+8H+═2Cl-+5I2+4H2O;
②玻璃液封装置的作用是吸收残留的ClO2气体(避免碘的逸出),故答案为:吸收残留的ClO2气体(避免碘的逸出);
③V中加入的指示剂通常为淀粉溶液,滴定至终点的现象是溶液由蓝色变为无色,且半分钟内不变色,
故答案为:淀粉溶液;溶液由蓝色变为无色,且半分钟内溶液颜色不再改变;
④若要除去超标的亚氯酸盐,ac均不能还原亚氯酸盐,b中KI具有还原性但氧化产物不适合饮用水使用,只有d中Fe2+将ClO2-还原成Cl-,Fe2+ 被氧化为铁离子,且铁离子水解生成胶体可净化饮用水,则最适宜的是d,
故答案为:d.
点评 本题考查物质含量的测定,为高频考点,为2015年高考真题改编题,把握物质的性质、制备原理、发生的反应为解答的关键,侧重分析与实验能力的综合考查,综合性较强,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列家庭化学小实验不能达到预期目的是( )
| A. | 用醋、石灰水验证蛋壳中含有碳酸盐 | |
| B. | 用碘酒检验汽油中是否含有不饱和烃 | |
| C. | 用鸡蛋清、食盐、水完成蛋白质的溶解、盐析实验 | |
| D. | 用米汤检验食用加碘盐(含KIO3)中含有碘 |
16.制备硫酸亚铁铵晶体的实验中,下列有关说法不合理的是( )
| A. | 在烧杯中用热的饱和碳酸钠溶液洗涤铁屑后,用倾析法分离并洗涤铁屑 | |
| B. | 搅拌,小火加热混合溶液,在蒸发皿中蒸发浓缩至溶液表面出现晶膜为止 | |
| C. | 抽滤后用冰水洗涤晶体表面附着的杂质 | |
| D. | 结晶前的溶液浓度较小有利于得到较大颗粒的硫酸亚铁铵晶体 |
20.下列说法中正确的是( )
| A. | 等物质的量浓度的(NH4)2CO3溶液和(NH4)2SO4溶液中c(NH4+)相同 | |
| B. | FeCl3溶液不能与固体CaCO3发生反应 | |
| C. | 一定条件下,反应2Mg(s)+CO2(g)═C(s)+2MgO(s)具有自发性,其△H>0 | |
| D. | 将0.005mol Na2O2溶于水得到1L溶液,此溶液在常温下的pH=12 |
5.下列各组物质的晶体中,晶体类型、化学键类型均完全相同的是( )
| A. | SO2和SiO2 | B. | CCl4和KCl | C. | NaOH和CaCl2 | D. | CO2和H2S |
12.PH3是一种无色剧毒气体,分子结构和NH3相似.关于PH3的说法中错误的是( )
| A. | PH3分子呈三角锥形 | B. | PH3分子是极性分子 | ||
| C. | 键能:P-H>N-H | D. | PH3在空气中易自燃 |
9.下列化学用语正确的是( )
| A. | 羟基的电子式 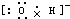 | |
| B. | F原子的轨道式 | |
| C. | 硫原子的电子排布式 1s22s22p63s23p6 | |
| D. | 氨气的结构式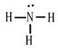 |
10.相同主族的短周期元素中,形成的单质一定属于相同类型晶体的是( )
| A. | 第IA族 | B. | 第IIIA族 | C. | 第IVA族 | D. | 第VIA族 |
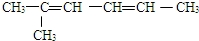 的名称为2-甲基-2,4-己二烯.
的名称为2-甲基-2,4-己二烯. .
.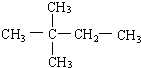 进行一氯取代反应后,只能生成3种沸点不同产物.
进行一氯取代反应后,只能生成3种沸点不同产物.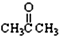 ③CH3CH2Br④
③CH3CH2Br④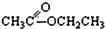 ⑤
⑤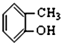 ⑥
⑥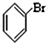 ⑦
⑦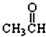 ⑧
⑧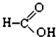 ⑨
⑨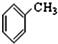 ⑩
⑩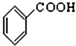
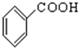 +CH3CH2OH$?_{浓硫酸}^{△}$
+CH3CH2OH$?_{浓硫酸}^{△}$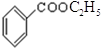 +H2O.
+H2O.