题目内容
6.下列有关物质的用途正确的是( )| A. | NaHCO3可以用于治疗胃酸过多 | |
| B. | 浓硝酸具有强氧化性,因此浓硝酸可以作为漂白剂 | |
| C. | SiO2可以用于生产太阳能电池 | |
| D. | 在FeCl3饱和溶液里通入足量NH3可制取Fe(OH)3胶体 |
分析 A.碳酸氢钠和盐酸反应,可用于中和胃酸;
B.浓硝酸具有强腐蚀性,易挥发不能做漂白剂;
C.SiO2应用于光导纤维,高纯硅用于太阳能电池;
D.在FeCl3饱和溶液里通入足量NH3可反应得到氢氧化铁沉淀.
解答 解:A.碳酸氢钠溶液碱性较弱,NaHCO3与胃酸中的盐酸反应,可用于治疗胃酸过多,故A正确;
B.浓硝酸具有强腐蚀性,被还原生成有毒气体二氧化氮,能使一些有色物质褪色,但不能做漂白剂,故B错误;
C.高纯硅为半导体,常用作制造太阳能电池的原料,二氧化硅是制备光导纤维的原料,故C错误;
D.氢氧化铁胶体制备是在沸水中滴加饱和氯化铁溶液,加热至红褐色得到氢氧化铁胶体,在FeCl3饱和溶液里通入足量NH3不能制取Fe(OH)3胶体,故D错误;
故选A.
点评 本题考查常见物质的性质及用途,题目难度不大,性质决定用途,注意常见相关基础知识的积累.

练习册系列答案
相关题目
10.下列物质只含有非极性键的是( )
| A. | H2O | B. | HCl | C. | NaOH | D. | O2 |
14.根据下列三个反应的化学方程式,判断有关物质的还原性的强弱顺序( )
①I2+SO2+2H2O═H2SO4+2HI
②2FeCl2+Cl2═2FeCl3
③2FeCl3+2HI═2FeCl2+I2+2HCl.
①I2+SO2+2H2O═H2SO4+2HI
②2FeCl2+Cl2═2FeCl3
③2FeCl3+2HI═2FeCl2+I2+2HCl.
| A. | I->Fe2+>Cl->SO2 | B. | Cl->Fe2+>SO2>I- | ||
| C. | Fe2+>I->Cl->Cl->SO2 | D. | SO2>I->Fe2+>Cl- |
1.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O
对于该反应,下列说法正确的是( )
2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O
对于该反应,下列说法正确的是( )
| A. | 水是还原产物 | B. | Fe(OH)3发生还原反应 | ||
| C. | Cl2是氧化剂 | D. | 每生成1mol K2FeO4转移2mol电子 |
18.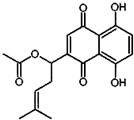 乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是( )
乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是( )
 乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是( )
乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是( )| A. | 该分子中含有1个手性碳原子 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1mol 乙酰紫草素最多可与2molBr2反应 | |
| D. | 1mol乙酰紫草素最多可与2molNaOH反应 |
15.下列有关物质的应用不恰当的是( )
| A. | 氧化铝可用作耐火材料 | B. | 氧化铁可用作红色油漆和涂料 | ||
| C. | 浓氨水可检验氯气管道漏气 | D. | 二氧化硫可用于食品增白 |
16.下列实验中的试剂b不可能是( )


| A. | NaOH | B. | H2O2 | C. | HCl | D. | AgNO3 |
