题目内容
15.对于反应2SO2(g)+O2(g)?2SO3(g),下列措施能增大反应速率的是( )①恒容条件下,再通入一定量的O2
②增大体系容积
③恒容条件下,再通入一定量的N2
④使用合适的催化剂.
| A. | ①④ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
分析 一般来说,增大反应速率,可增大浓度,升高温度,增大压强,或加入催化剂等,以此解答该题.
解答 解:①恒容条件下,再通入一定量的O2,浓度增大,则反应速率增大,故正确;
②增大体系容积,浓度减小,反应速率减小,故错误;
③恒容条件下,再通入一定量的N2,不参加反应,气体浓度不变,反应速率不变,故错误;
④使用合适的催化剂,可增大反应速率,
故选A.
点评 本题考查化学反应速率的影响因素,侧重于学生的分析能力的考查,为高考高频考点,注意把握影响反应速率的因素,注重相关知识的学习与积累,难度不大.

练习册系列答案
相关题目
17.对反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列结论正确的是( )
| A. | FeS2只作还原剂 | |
| B. | 只有CuSO4作氧化剂 | |
| C. | 1 mol CuSO4可以氧化$\frac{5}{7}$ mol硫元素 | |
| D. | 被氧化的硫和被还原的硫的质量之比为3:7 |
18.下列实验操作中溶液里无固体析出的是( )
| A. | CuCl2溶液中加入钠的小颗粒 | |
| B. | 饱和的Ca(OH)2溶液中加入钠的小颗粒 | |
| C. | NaOH的饱和溶液中加入钠的小颗粒 | |
| D. | 稀硫酸中加入钠的小颗粒 |
3.如图药品和装置合理且能完成相应实验的是( )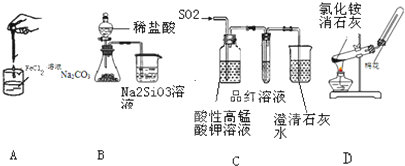

| A. | 制备氢氧化亚铁 | B. | 验证非金属性Cl>C>Si | ||
| C. | 检验二氧化硫中是否混有二氧化碳 | D. | 实验室制取并收集氨气 |
7.下列离子方程式书写正确的是( )
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | 将过量的SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O═HClO+HSO3- | |
| C. | 向MgSO4溶液中滴加Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O |
4.含有共价键的离子化合物是( )
| A. | HCl | B. | NaOH | C. | Na2O | D. | CH4 |
5.下列物质在生活中应用时,起还原作用的是( )
| A. | 明矾作净水剂 | B. | 甘油作护肤保湿剂 | ||
| C. | 铁粉作食品袋内的脱氧剂 | D. | “84消毒液”杀菌消毒 |

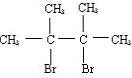
 .
.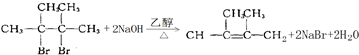 .
.