题目内容
要除去Na2CO3溶液中含有的少量NaHCO3杂质,所选试剂最好是( )
| A、澄清的石灰水 |
| B、Ba(OH)2溶液 |
| C、NaOH溶液 |
| D、盐酸 |
考点:钠的重要化合物,物质的分离、提纯和除杂
专题:几种重要的金属及其化合物
分析:溶液中Na2CO3能与CO2、H2O反应生成NaHCO3,NaHCO3与CO2不反应,所以可用通入CO2来除杂,以此解答.
解答:
解:A.加入Ca(OH)2溶液,氢氧化钙和碳酸氢钠反应,同时也能和碳酸钠反应,反应掉主要成分,同时引入新杂质NaOH,不能达到除杂目的,故A错误;
B.加入氢氧化钡溶液,氢氧化钡和碳酸氢钠反应,同时也能和碳酸钠反应,反应掉主要成分,同时引入新杂质NaOH,不能达到除杂目的,故B错误;
C.加入适量的氢氧化钠溶液,碳酸氢钠与氢氧化钠发生了反应生成碳酸钠和水,杂质转化为主要成分,故C正确;
D.加入盐酸,盐酸和碳酸氢钠反应,同时也能和碳酸钠反应,反应掉主要成分,同时引入新杂质NaCl,不能达到除杂目的,故D错误;
故选C.
B.加入氢氧化钡溶液,氢氧化钡和碳酸氢钠反应,同时也能和碳酸钠反应,反应掉主要成分,同时引入新杂质NaOH,不能达到除杂目的,故B错误;
C.加入适量的氢氧化钠溶液,碳酸氢钠与氢氧化钠发生了反应生成碳酸钠和水,杂质转化为主要成分,故C正确;
D.加入盐酸,盐酸和碳酸氢钠反应,同时也能和碳酸钠反应,反应掉主要成分,同时引入新杂质NaCl,不能达到除杂目的,故D错误;
故选C.
点评:本题考查的是物质的除杂,主要考查碳酸钠与碳酸氢钠的化学性质,侧重于学生的分析能力和实验能力的考查,注意根据除杂质的两个条件综合把握,问题就会迎刃而解,题目难度不大.

练习册系列答案
相关题目
将铁片和银片用导线连接置于同一稀盐酸中,经过一段时间后,下列叙述正确的是( )
| A、负极有Cl2逸出,正极有H2逸出 |
| B、负极附近Cl-的浓度逐渐减小 |
| C、正极附近Cl-的浓度逐渐增大 |
| D、溶液中Cl-的浓度基本不变 |
下列关于胶体的叙述,正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径大于10-7m |
| B、制备氢氧化铁胶体的化学方程式是:FeCl3+3H2O═Fe(OH)3↓+3HCl |
| C、用平行光照射NaCl溶液和氢氧化铁胶体时,产生的现象相同 |
| D、氢氧化铁胶体能够使水中悬浮的固体颗粒沉降,达到净水的目的 |
白铁皮发生吸氢腐蚀时,若有0.2mol电子发生转移,下列说法中正确的是( )
| A、有6.5g锌被腐蚀 |
| B、标况下生成22.4L氢气 |
| C、有2.8g锌被腐蚀 |
| D、标况下生成2.24L氢气 |
设NA 为阿伏伽德罗常数的数值,下列说法不正确的是( )
| A、39gC2H2和C6H6混合物中含有的原子数为6NA |
| B、标准状况下,以任意比例混和的CO和C2H4混和物22.4L,所含有的原子数为2NA |
| C、23g甲酸中所含的共用电子对数为2.5NA |
| D、7.1gCl2与足量的NaOH溶液发生反应,电子转移数为0.1 NA |
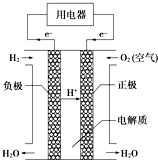 上海世博会有千辆氢氧燃料电池车上路,参看某种氢氧燃料电池原理图,下列说法不正确的是( )
上海世博会有千辆氢氧燃料电池车上路,参看某种氢氧燃料电池原理图,下列说法不正确的是( )| A、氢氧燃料电池是一种具有应用前景的绿色电源 |
| B、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
| C、氢氧燃料电池能量转换率比氢气直接燃烧高 |
| D、氢氧燃料电池工作时,发出淡蓝色火焰 |
常温下,四个容积为20L的容器中分别装有下列气体,产生的压强最大的是( )
| A、5 gH2 |
| B、24 gHCl |
| C、48 g SO2 |
| D、55 g CO2 |
下列物质不能发生水解反应的是( )?
| A、蛋白质 | B、油脂 |
| C、蔗糖 | D、葡萄糖 |