题目内容
20.根据元素的单质和化合物性质判断元素非金属性强弱的依据是( )| A. | 元素最高价氧化物的水化物的碱性强弱 | |
| B. | 元素最高价氧化物的水化物的酸性强弱 | |
| C. | 元素单质跟酸反应置换出氢的难易 | |
| D. | 元素单质跟氢气生成气态氢化物的难易 |
分析 比较非金属性的强弱,可根据①最高价氧化物对应水化物的酸性强弱,②与氢气反应的剧烈程度,③氢化物的稳定性,④单质之间的置换反应等,⑤对应阴离子的还原性强弱等.
解答 解:A.比较元素的非金属性强弱,可根据最高价氧化物对应水化物的酸性强弱,比较元素的金属性强弱,可根据最高价氧化物对应水化物的碱性强弱,故A错误;
B.比较元素的非金属性强弱,可根据最高价氧化物对应水化物的酸性强弱,故B正确;
C.非金属性元素不能与酸发生置换反应生成氢气,比较方法错误,故C错误;
D.元素的非金属性越强,元素对应的单质越易与氢气发生化合反应,故D正确.
故选BD.
点评 本题考查元素非金属性的比较,题目难度不大,本题注意把握比较非金属性的方法,侧重于考查学生的分析能力.

练习册系列答案
相关题目
10.下列有关金属的说法中正确的是( )
| A. | 铝在空气中能生成一层致密的氧化物保护膜 | |
| B. | 铜的化学性质不活泼,在潮湿的空气中也不生锈 | |
| C. | 钛具有耐腐蚀性,可用来制造海轮的外壳 | |
| D. | 镀锌的“白铁皮”不易生锈,说明锌没有铁活泼 |
11.下列溶液中有关物质的量浓度关系或计算正确的是( )
| A. | pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有:C(NaOH)<C(CH3COONa)<C(NaHCO3) | |
| B. | 25℃时,0.1 mol•L-1 Na2CO3溶液中水电离出来的C(OH-)大于0.1 mol•L-1 NaOH溶液中水电离出来的C(OH-) | |
| C. | 常温下物质的量浓度相等的①(NH4)2Fe(SO4)2②(NH4 )2CO3;③(NH4)2SO4三种溶液中c(NH4+):①>②>③ | |
| D. | 室温下,0.1 mol•L-1 NaHA溶液的pH=4,则C(HA-)>C(H+)>C(H2A)>C(A2ˉ) |
8.乙炔和苯的混合物13g完全燃烧后生成CO2和H2O,消耗氧气的质量为( )
| A. | 40g | B. | 20g | C. | 32g | D. | 无法计算 |
15.下列实验操作或描述中正确的是( )
| A. | 氧化铁与足量盐酸反应后的溶液中滴加硫氰化钾溶液会生成血红色沉淀 | |
| B. | 配制溶液定容时,应将烧杯中蒸馏水缓缓地注入到容量瓶中,直到溶液的凹液面正好与刻度线相切,再将容量瓶塞盖好,反复上下颠倒摇匀 | |
| C. | 用元素分析仪可确定物质中是否含C、H、O、N、S、Cl、Br等元素,用红外光谱仪可确定物质中是否存在某些有机原子团,用原子吸收光谱可确定物质中含哪些金属元素等 | |
| D. | 观察钾元素焰色反应的操作是:将铂丝在稀盐酸中洗涤后直接蘸取固体氯化钾,置于酒精灯火焰上进行灼烧,观察火焰是否显紫色来确定 |
5.在平衡体系Ca(OH)2(s)?Ca2++2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是( )
| A. | 加入少量MgCl2固体 | B. | 加入少量Na2CO3固体 | ||
| C. | 加入少量KCl固体 | D. | 加入少量稀H2SO4 |
12.关于如图所示结构简式的说法正确的是( )
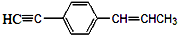

| A. | 所有碳原子不可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有6个碳原子可能在同一直线上 | |
| D. | 只可能有5个碳原子在同一直线上 |
9.下列各物质中,属于电解质的是( )
| A. | 盐酸 | B. | 硫酸钡 | C. | 蔗糖 | D. | 浓氨水 |
10.下列实验现象与结论均正确的是( )
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向未知液中滴加氯水,再滴加KSCN溶液 | 溶液呈红色 | 未知液中一定含有Fe2+ |
| B | 向无色溶液中滴加氯水,再加CCl4振荡,静置 | 溶液分层,下层呈紫红色 | 无色溶液中一定含I- |
| C | 某气体通入品红溶液中 | 红色褪去 | 该气体中一定含SO2 |
| D | 将豆粒大金属钾投入水中 | 钾熔化成小球,在水面上游动 | 金属钾密度一定小于水 |
| A. | A | B. | B | C. | C | D. | D |