题目内容
1.下列说法正确的是( )| A. | 难溶物在水中的溶解度为0 | |
| B. | 绝对不溶解的物质是不存在的 | |
| C. | 难溶物是指物质不溶于水 | |
| D. | 某离子被沉淀完全是指该离子在溶液中的浓度为0 |
分析 一般来说,物质的溶度积越小,则溶解度越小,当浓度小于10-5mol/L时可认为完全溶解,可利用沉淀的转化除杂,以此解答该题.
解答 解:某物质的溶解性为难溶,则该物质的溶解度小于0.1g,难溶是相对的,不溶的物质不存在,当浓度≤1×10-5mol/L时,可认为完全沉淀,只有B正确.
故选B.
点评 本题考查溶解度含义与影响因素等,为高频考点,难度不大,注意溶解度、溶度积意义以及异同点,明确物质的溶解度与溶度积的关系及化学平衡移动原理适用于沉淀溶解平衡即可解答,注意难溶是相对的,题目难度不大.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
20.能正确表示下列反应的离子方程式是( )
| A. | FeO与稀硝酸反应:FeO+2H+═Fe2++H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 向碳酸钠溶液中逐滴加入等体积等物质的量浓度的稀醋酸:CO32-+H+═HCO3- |
12.下列物质的应用或转化与氧化还原反应原理有关的是( )
| A. | 利用铝热反应焊接铁轨 | B. | 用稀盐酸除去水垢 | ||
| C. | 用胃舒平(氢氧化铝)治疗胃酸过多 | D. | 工业上煅烧石灰石制生石灰 |
9.25℃时,两种浓度不同的NaOH溶液,c(H+)分别为1.0×10-14 mol•L-1和1.0×10-12 mol•L-1,将这两种溶液等体积混合后,所得溶液的pH约为(提示:lg2≈0.3,lg5≈0.7)( )
| A. | 14 | B. | 13.7 | C. | 13 | D. | 12.7 |
16.下列反应中,既属于氧化还原反应又属于置换反应的是( )
| A. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O | B. | CO2+Ca(OH)2═CaCO3↓+H2O | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | D. | 2Na+Cl2═2NaCl |
6.以下实验能获得成功的是( )
| A. | 用溴水鉴别苯和甲苯 | |
| B. | 用酸性高锰酸钾溶液区分苯和已烷 | |
| C. | 将铁屑、溴水、苯混合制溴苯 | |
| D. | 用苯乙烯在合适条件下催化加氢制备乙基环已烷 |
13.下列装置中,能构成原电池的是( )
| A. | 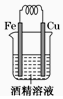 | B. | 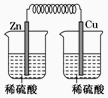 | C. | 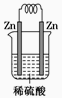 | D. | 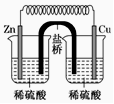 |
10.下列有关实验操作的解释或结论正确的是( )
| 选项 | 实验操作 | 解释或结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2的 |
| B | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| C | 测定中和热时,使用碎泡沫起隔热保温的作用,用普通玻璃棒进行搅拌使酸和碱充分反应,准确读取实验时的最高温度并且取2~3次的实验平均值等,以达到良好的实验效果 | 用简易量热计测定反应热 |
| D | 用氢氧化钾与浓硫酸测定中和反应的反应热 | 测得的结果偏小 |
| A. | A | B. | B | C. | C | D. | D |
6.CO(g)+H2O(g)?H2(g)+CO2(g)△H<0,在其他条件不变的情况下,下列说法正确的是( )
| A. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| B. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| C. | 升高温度,反应速率加快,反应放出的热量不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |