题目内容
8.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 0.5mol?L-1K2SO4含有的K+数目为NA | |
| B. | 56g铁与足量的盐酸反应时失去电子的数目为3NA | |
| C. | 在标准状况下,22.4LCCl4中含有的分子数目为NA | |
| D. | 在常温常压下,16gO2和O3的混合气体所含原子数目为NA |
分析 A.缺少硫酸钾的体积,无法计算硫酸钾的物质的量;
B.铁与盐酸反应生成氯化亚铁,56g铁的物质的量为1mol,完全反应失去2mol电子;
C.标准状况下,四氯化碳的状态不是气体;
D.氧气和臭氧中都只含有氧元素,16g氧气和臭氧的混合物中含有16个氧原子,根据n=$\frac{n}{M}$计算出含有的氧原子数目.
解答 解:A.没有告诉硫酸钾溶液的体积,无法计算溶液中含有钾离子的物质的量及数目,故A错误;
B.56g铁的物质的量为:$\frac{56g}{56g/mol}$=1mol,1molFe与足量的盐酸反应时失去2mol电子,失去电子的数目为2NA,故B错误;
C.标准状况下,四氯化碳不是气体,不能使用标准状况下的气体摩尔体积计算,故C错误;
D.16gO2和O3的混合气体中含有16个氧原子,含有氧原子的物质的量为:$\frac{16g}{16g/mol}$=1mol,所含原子数目为NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,明确标准状况下气体摩尔体积的使用条件.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.CO可用于炼铁,已知:
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1;则CO还原Fe2O3(s)的热化学方程式为( )
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1;则CO还原Fe2O3(s)的热化学方程式为( )
| A. | Fe2O3+3CO=═2Fe+3CO2△H=-28.5 kJ•mol-1 | |
| B. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ | |
| C. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=+28.5 kJ•mol-1 | |
| D. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1 |
19.下列实验方案不合理的是( )
| A. | 用KSCN溶液检验FeCl2是否已被氧化而变质 | |
| B. | 用焰色反应鉴别NaCl和KCl | |
| C. | 用加热法除去Na2CO3中混有的NaHCO3杂质 | |
| D. | 用NaOH溶液除去MgCl2溶液中的CuCl2杂质 |
16.2015年8月12日位于天津滨海新区某一危险品仓库发生大爆炸,人员和财产损失严重.为此我们应做好各类安全预案.下列行为符合安全要求的是( )
| A. | 金属钠着火时,立即用水灭火 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中 | |
| C. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处走 |
3.下列反应的离子方程式书写正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| B. | 大理石投入稀硝酸中:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氨水与硫酸铝溶液混合:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | |
| D. | 氯水通入水中:Cl2+H2O═Cl-+ClO-+2H+ |
20.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),如表各组物质中不能按图示关系转化的是( )
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A | 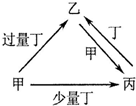 | NaOH | NaHCO3 | Na2CO3 | CO2 |
| B | C | CO | CO2 | O2 | |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
| D | AlCl3 | NaAlO2 | Al(OH)3 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
17.按要求回答下列问题:
(1)实验室常用NaOH溶液来进行洗气和提纯,当100mL3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变
D.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$减小
(3)①常温下将0.15mol/L稀硫酸V1mL与0.1mol/LNaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积变化忽略不计).
②常温下若溶液由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是AD
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如表所示:
①根据表中数据,将浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最小的是A.
A.HCN B.HClO C.Na2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+CO2+H2O
(5)几种离子开始沉淀时的pH如下表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,Cu2+(填离子符号)先沉淀,Ksp[Fe(OH)2]<Ksp[Mg(OH)2](填“>”、“=”或“<”)
(1)实验室常用NaOH溶液来进行洗气和提纯,当100mL3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减小
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变
D.溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$减小
(3)①常温下将0.15mol/L稀硫酸V1mL与0.1mol/LNaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积变化忽略不计).
②常温下若溶液由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是AD
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.Na2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.NaHCO3+HCN═NaCN+CO2+H2O
(5)几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
18.某无色透明的溶液中,能大量共存的离子组是( )
| A. | Na+、Cu2+、SO42-、OH- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | K+、Ca2+、Cl-、MnO4- | D. | Na+、CO32-、SO42-、H+ |