题目内容
将NaHCO3置于干的试管中加热,并使放出的气体依次通过盛有足量过氧化钠和碱石灰的干燥管,最后得到的气体有( )
| A、CO2、H2O |
| B、H2O、O2 |
| C、CO2、O2 |
| D、O2 |
考点:钠的重要化合物
专题:元素及其化合物
分析:碳酸氢钠不稳定受热容易分解,生成二氧化碳和水,二氧化碳和水蒸气都能与过氧化钠反应生成氧气,过量的二氧化碳与氢氧化钙反应被吸收,最终剩余气体为氧气,据此解答.
解答:
解:碳酸氢钠不稳定受热分解:2NaHCO3
Na2CO3+H2O+CO2↑,分解生成的二氧化碳和水与过量的过氧化钠发生反应:2Na2O2+2CO2═2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑,反应生成氧气,因为过氧化钠和碱石灰足量,可以完全吸收二氧化碳和水,所以最终剩余气体为氧气;
故选:D.
| ||
故选:D.
点评:本题考查了碳酸氢钠、过氧化钠的性质,题目不难,属于基础题,熟悉二者的化学性质是解题关键.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
我国推广使用乙醇汽油,它是在汽油中加入适量乙醇形成的混合燃料.下列叙述中正确的是( )
| A、使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源 |
| B、燃料中的乙醇可以通过粮食发酵或化工合成等方法制得 |
| C、乙醇汽油是一种新型化合物 |
| D、燃烧乙醇汽油可以减少对大气的污染是因为它不含硫元素和氮元素 |
下列物质的溶液中所含离子种类最多的是( )
| A、H2S |
| B、Na3PO4 |
| C、NaHCO3 |
| D、AlCl3 |
乙酸的分子结构为 ,下列关于反应与断键部位叙述正确的是( )
,下列关于反应与断键部位叙述正确的是( )
(1)乙酸与乙醇发生酯化反应时,②键断裂
(2)乙酸的电离以及与酸的通性有关的反应,是③键断裂
(3)在红磷存在时,Br2可与CH3COOH发生反应:Br2+CH3COOH
CH2Br-COOH+HBr,是③键断裂
(4)乙酸变成乙酸酐的反应:2CH3COOH→ +H2O,是①②键断裂.
+H2O,是①②键断裂.
 ,下列关于反应与断键部位叙述正确的是( )
,下列关于反应与断键部位叙述正确的是( )(1)乙酸与乙醇发生酯化反应时,②键断裂
(2)乙酸的电离以及与酸的通性有关的反应,是③键断裂
(3)在红磷存在时,Br2可与CH3COOH发生反应:Br2+CH3COOH
| 红磷 |
(4)乙酸变成乙酸酐的反应:2CH3COOH→
 +H2O,是①②键断裂.
+H2O,是①②键断裂.| A、(1)(2)(3) |
| B、(2)(3)(4) |
| C、(1)(3)(4) |
| D、(1)(2)(4) |
在一定温度下,下列叙述不是可逆反应A(气)+3B(气)?4C(气)+D(固)达到平衡的标志的是( )
①C的生成 速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A的转化率不变
⑤混合气体的总压强不再变化
⑥气体的平均摩尔质量保持不变
⑦A、B、C、D的分子数之比为1:3:2:2
⑧同温同容下,气体的密度保持不变.
①C的生成 速率与C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A的转化率不变
⑤混合气体的总压强不再变化
⑥气体的平均摩尔质量保持不变
⑦A、B、C、D的分子数之比为1:3:2:2
⑧同温同容下,气体的密度保持不变.
| A、②⑤ | B、②⑤⑧ |
| C、①③④⑦ | D、②⑤⑦ |
下列溶液,pH>7的是( )
| A、KNO3 |
| B、CH3COONa |
| C、NaHSO4 |
| D、AlCl3 |
下列离子方程式书写正确的是( )
| A、铁跟盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、向氯化铝溶液中通入氨气至过量:4NH3+Al3++2H2O=AlO2-+4NH4+ |
| C、次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2=HCO3-+HClO |
| D、碳酸钙与盐酸反应CO32-+2H+=CO2↑+H2O |
将二氧化碳通入Ba(OH)2稀溶液中,能正确表示其导电能力变化的是( )
A、 |
B、 |
C、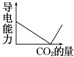 |
D、 |