题目内容
5.下列表示钠原子的式子中能反映能级差别和电子自旋状态的是( )| A. |  | B. | $\stackrel{23}{11}$Na | ||
| C. | 1s22s22p63s1 | D. | 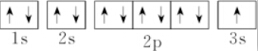 |
分析 A.原子结构示意图中只有电子层,没有电子亚层;
B.原子符号中没有电子排布;
C.电子排布式中含有电子层和电子亚层,但是不能看出电子自旋状态;
D.电子排布图中包含了电子层和电子亚层,以及电子自旋状态.
解答 解:A.原子结构示意图中只有电子层,没有电子亚层,不能看出电子自旋状态,故A错误;
B.$\stackrel{23}{11}$Na中只能知道Na含有11个电子,不能反映能级差别和电子自旋状态,故B错误;
C.电子排布式中含有电子层和电子亚层,能看出电子的能级差别,但是不能看出电子自旋状态,故C错误;
D.电子排布图中包含了电子层和电子亚层,小方块表示了能级差别,方块中的箭头表示电子自旋状态,故D正确.
故选D.
点评 本题考查了电子排布、原子结构示意图、原子符号的表示,题目难度不大,注意把握原子的表示方法和电子排布规律.

练习册系列答案
相关题目
13.不用其它试剂鉴别(1)KOH (2)NaCl (3)MgSO4 (4)Cu(NO3)2四种溶液,正确的鉴别顺序是( )
| A. | (1)(4)(3)(2) | B. | (4)(1)(3)(2) | C. | (4)(2)(1)(3) | D. | (1)(3)(4)(2) |
20.某温度时,2NO(g)+O2(g)═2NO2(g)反应到2s后,NO的浓度减少了0.06mol•L-1,则以O2表示该时段的化学反应速率是( )
| A. | 0.03mol•L-1•s-1 | B. | 0.015mol•L-1•s-1 | ||
| C. | 0.12mol•L-1•s-1 | D. | 0.06mol•L-1•s-1 |
10.下列依据相关实验得出的结论正确的是( )
| A. | 向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊的气体,该溶液中一定含有CO32- | |
| B. | 向某溶液中滴加氯水,再加入KSCN溶液,溶液变红,该溶液中一定含有Fe2+ | |
| C. | 向某溶液中通入Cl2后,溶液变黄,继续加淀粉溶液,溶液变蓝,说明原溶液中有I- | |
| D. | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
17.下图所示对实验仪器名称的标注或实验操作正确的是( )
| A. |  实验室制氯气 实验室制氯气 | B. |  氨气的制取 氨气的制取 | ||
| C. |  Fe(OH)2的制取 Fe(OH)2的制取 | D. |  浓硫酸的稀释 浓硫酸的稀释 |
15.下列有关热化学方程式的书写及对应的表述均正确的是( )
| A. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸与0.1 mol•L-1 NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热△H=-110.5 kJ•mol-1 |
 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题: