题目内容
3.在酸性条件下,过氧化氢可以与高锰酸钾溶液反应,离子方程式如下(未配平):_____MnO4-____H2O2+_____H+=____ Mn2++_____O2↑+_____H2O
下列说法错误的是( )
| A. | Mn2+的还原性弱于H2O2 | |
| B. | MnO4-是氧化剂,O2是氧化产物 | |
| C. | 生成lmol O2时,转移4 mol电子 | |
| D. | 离子方程式中按物质顺序的化学计量数是2、5、6、2、5、8 |
分析 该反应中,锰元素的化合价由+7价变为+2价,O元素的化合价由-1价变为0价,
A.同一自发进行的氧化还原反应中,还原剂的还原性大于还原产物的还原性;
B.得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,氧化剂对应的产物是还原产物;
C.根据氧气和转移电子之间的关系式计算;
D.根据化合价的变化和原子守恒配平.
解答 解:该反应中,锰元素的化合价由+7价变为+2价,O元素的化合价由-1价变为0价,
A.该反应中还原剂是H2O2,还原产物是Mn2+,还原剂的还原性大于还原产物的还原性,H2O2的还原性强于Mn2+,故A正确;
B.该反应中还原剂是H2O2,O2是氧化产物,MnO4-是氧化剂,故B正确;
C.H2O2被氧化为O2,化合价从-1价升高到0价,生成lmol O2时,转移2 mol电子,故C错误;
D.该反应中,锰元素的化合价由+7价变为+2价,O元素的化合价由-1价变为0价,则配平方程式为2MnO4-+5H2O2+6H+=2 Mn2++5O2↑+8H2O,故D正确;
故选C.
点评 本题考查了氧化还原反应,明确元素化合价变化是解本题关键,根据基本概念来分析解答,难度不大,侧重于基础知识的考查.

练习册系列答案
相关题目
13.20mL浓硝酸和2.56g铜反应,铜完全溶解,生成的气体颜色由深变浅(生成NO2、NO),共收集到1.12L气体(标准状况),剩余酸用NaOH中和,共耗去1mol/L氢氧化钠30mL.则浓HNO3物质的量浓度为( )
| A. | 8 mol/L | B. | 9 mol/L | C. | 11 mol/L | D. | 12 mol/L |
14.在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:
①FeCl2
②Fe2O3
③Zn
④Fe2(SO)3
⑤AgNO3
可使铜粉溶解的是( )
①FeCl2
②Fe2O3
③Zn
④Fe2(SO)3
⑤AgNO3
可使铜粉溶解的是( )
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ②④⑤ |
11.下列说法中正确的是( )
| A. | CuCl2溶液蒸干灼烧后得到CuCl2固体 | |
| B. | 火力发电的目的是使化学能转换为电能 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性. | |
| D. | 将FeCl3固体溶于适量蒸馏水来配制FeCl3溶液 |
18.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 0.5mol/L碳酸钠溶液中含有lmolNa+ | |
| B. | 14g氮气和一氧化碳混合气体中含原子总数为NA | |
| C. | 标准状况下,2.24LCCl4物质的量为0.1mol | |
| D. | 56g铁溶于过量的盐酸,电子转移数为3NA |
8.下列实验操作中正确的是( )
| A. | 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 分液操作时,静置分层后要先放出分液漏斗中下层液体,再倒出上层液体 | |
| C. | 分液操作时,选择的萃取剂的密度必须比水大 | |
| D. | 用胶头滴管向试管滴加液体时,滴管尖端靠在试管内壁 |
15.某下组同学欲研究SO2的性质.
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
(2)利用如图所示的装置研究SO2的性质:
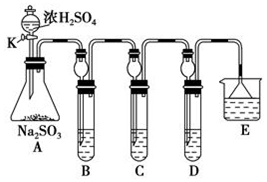
①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO4、Na2SO3、NaHSO3 | SO3、X、Na2SO4、NaHSO4 |

①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.
6.Na2S2O3•5H2O(俗称海波)是照相业常用的一种定影剂,常采用下法制备:将亚硫酸钠溶液与硫粉混合共热,生成硫代硫酸钠Na2SO3+S$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3,滤去硫粉,再将滤液浓缩、冷却,即有Na2S2O3•5H2O晶体析出.该法制得的晶体中常混有少量Na2SO3和Na2SO4的杂质.为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的H2SO4溶液20mL,充分反应后滤出硫,并将滤液微热(假定生成的SO2全部逸出),测得有关实验数据如下(标准状况):
(1)样品与硫酸可能发生反应的离子方程式为S2O32-+2H+=S↓+SO2↑+H2O、SO32-+2H+=SO2↑+H2O.
(2)根据上表数据分析,该样品A(填选项字母)
A.含有Na2S2O3、Na2SO3和Na2SO4三种成分
B.含有Na2S2O3和Na2SO3两种成分
C.只含有Na2S2O3
(3)求第三份样品中各成分的物质的量.
(4)求所加硫酸的物质的量浓度.
(5)若将63g该样品与一定量的该硫酸溶液微热,回答问题:
①欲计算生成SO2的体积,还需要提供的一个数据是(用a表示该数值,并注明单位)硫酸溶液的体积.当a=0.06时,V(SO2)=5.6;
②(2分)在图1上画出b随a变化的曲线
(6)图2是实验室制取SO2并验证SO2的某些性质的装置图.
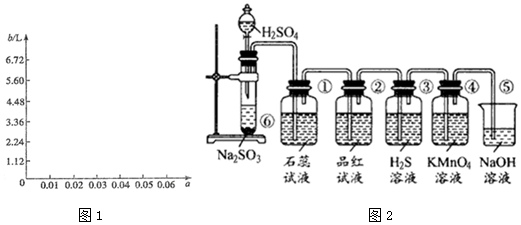
试回答:
Ⅰ.实验中应该选择浓硫酸,是否使用98%的浓H2SO4否(填“是”或“否”),写出⑥中反应化学反应方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑.
Ⅱ.①中的实验现象为变红.
Ⅲ.②中的现象证明SO2具有的化学性质为漂白性.
Ⅳ.③中的实验现象是变浑浊(生成淡黄色沉淀),证明SO2有氧化性.
Ⅴ.④中的实验现象是紫红色褪去,证明SO2有还原性.
Ⅵ.⑤的作用是吸收多余的SO2,防止污染空气.
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 12.60 | 18.90 | 28.98 |
| 二氧化硫的体积/L | 1.12 | 1.68 | 2.24 |
| 硫的质量/g | 1.28 | 1.92 | 2.56 |
(2)根据上表数据分析,该样品A(填选项字母)
A.含有Na2S2O3、Na2SO3和Na2SO4三种成分
B.含有Na2S2O3和Na2SO3两种成分
C.只含有Na2S2O3
(3)求第三份样品中各成分的物质的量.
(4)求所加硫酸的物质的量浓度.
(5)若将63g该样品与一定量的该硫酸溶液微热,回答问题:
①欲计算生成SO2的体积,还需要提供的一个数据是(用a表示该数值,并注明单位)硫酸溶液的体积.当a=0.06时,V(SO2)=5.6;
②(2分)在图1上画出b随a变化的曲线
(6)图2是实验室制取SO2并验证SO2的某些性质的装置图.

试回答:
Ⅰ.实验中应该选择浓硫酸,是否使用98%的浓H2SO4否(填“是”或“否”),写出⑥中反应化学反应方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑.
Ⅱ.①中的实验现象为变红.
Ⅲ.②中的现象证明SO2具有的化学性质为漂白性.
Ⅳ.③中的实验现象是变浑浊(生成淡黄色沉淀),证明SO2有氧化性.
Ⅴ.④中的实验现象是紫红色褪去,证明SO2有还原性.
Ⅵ.⑤的作用是吸收多余的SO2,防止污染空气.