题目内容
14.将250mLH2SO4的质量分数为98%,密度为1.84g/cm3的浓硫酸稀释到1000mL.①原浓H2SO4的物质的量浓度为18.4mol/L;
②此时溶液中H+的物质的量浓度为9.2mol/L.
分析 ①浓硫酸物质的量浓度=$\frac{1000ρω}{M}$;
②稀释前后溶质的物质的量不变,据此计算稀释后稀硫酸物质的量浓度,氢离子浓度是硫酸的2倍,据此计算稀释后氢离子浓度.
解答 解:①浓硫酸物质的量浓度=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
故答案为:18.4mol/L;
②稀释前后溶质的物质的量不变,则稀释后硫酸物质的量浓度=$\frac{18.4mol/L×0.25L}{1L}$=4.6mol/L,硫酸溶液中氢离子浓度是硫酸的2倍,则稀释后氢离子浓度=4.6mol/L×2=9.2mol/L,
故答案为:9.2mol/L.
点评 本题考查物质的量浓度计算,为高频考点,明确各个物理量之间的关系式是解本题关键,侧重考查学生分析计算能力,注意密度、质量分数与物质的量浓度的关系,为易错题.

练习册系列答案
相关题目
4.根据图提供的信息,下列所得结论不正确的是( )
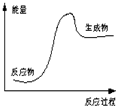

| A. | 该反应为吸热反应 | |
| B. | 该图可以表示石灰石高温分解 | |
| C. | 反应物比生成物稳定 | |
| D. | 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热 |
5.(1)下列变化中,①I2升华,②烧碱熔化,③NaCl溶于水,④HCl溶于水,⑤O2溶于水,⑥Na2O2溶于水.未发生化学键断裂的是①⑤;(填序号,下同)仅发生离子键断裂的是②③;仅发生共价键断裂的是④;即发生离子键断裂,又发生共价键断裂的是⑥;
(2)1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(3)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl.
(2)1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(3)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3 401 |
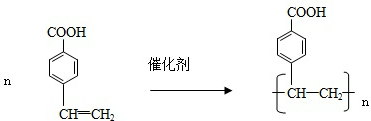
9.下列关于乙烯和聚乙烯的叙述不正确的是( )
| A. | 乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物 | |
| B. | 可以采用通过溴水洗气的方法以除去乙烷中的乙烯气体 | |
| C. | 乙烯和聚乙烯都能使溴水褪色 | |
| D. | 取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 |
3.有关化工生产的叙述正确的是( )
| A. | 联碱法对母液的处理方法是向母液中通入二氧化碳,冰冻和加食盐 | |
| B. | 列管式热交换器的使用实现了原料的充分利用 | |
| C. | 焙烧辰砂制取汞的反应原理为:HgS+O2$\stackrel{焙烧}{→}$Hg+SO2 | |
| D. | 氯碱工业、铝的冶炼、牺牲阳极的阴极保护法都是应用了电解池的原理 |
10.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质).
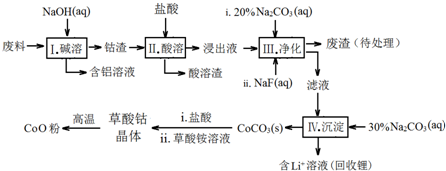
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应调节溶液的pH范围是3.2-7.15;废渣中的主要成分为Fe(OH)3、LiF.
(4)步骤Ⅲ中NaF参与的反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,[M (CoC2O4•2H2O)=183g/mol]受热过程中不同温度范围内分别得到一种固体物质,其质量如表.
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是3CoC2O4+2O2 $\frac{\underline{\;210℃-290℃\;}}{\;}$Co3O4+6CO2.

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应调节溶液的pH范围是3.2-7.15;废渣中的主要成分为Fe(OH)3、LiF.
(4)步骤Ⅲ中NaF参与的反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,[M (CoC2O4•2H2O)=183g/mol]受热过程中不同温度范围内分别得到一种固体物质,其质量如表.
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
 .
. .
. .
. .
.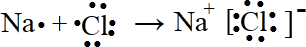 .
.