题目内容
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=IO+5I-+3H2O,下列说法不正确的是( )
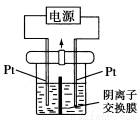
A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH-
B.电解结束时,右侧溶液中含有IO3-
C.电解槽内发生反应的总化学方程式:KI+3H2O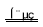 KIO3+3H2↑
KIO3+3H2↑
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变
D
【解析】
试题分析:在一定的电压下通电,发现左侧溶液变蓝色,则在左侧发生的的氧化反应:2I—-2e-=I2, I2,遇淀粉溶液变为蓝色,则在右侧发生的是还原反应,电极电极反应式:2H2O+2e-=H2↑+2OH-,正确;B.由于 在电解时阴离子在左侧失去电子被氧化为I2,阳离子H+在右侧放电产生氢气,所以所以在右侧c(OH-)浓度增大,发生反应3I2+6OH-=IO +5I-+3H2O,故电解结束时,右侧溶液中含有IO3-,错误;C.电解槽内左侧发生反应:2I—-2e-=I2;3I2+6OH-=IO
+5I-+3H2O,故电解结束时,右侧溶液中含有IO3-,错误;C.电解槽内左侧发生反应:2I—-2e-=I2;3I2+6OH-=IO +5I-+3H2O,左侧的总方程式是I—-6e-+6OH-=IO
+5I-+3H2O,左侧的总方程式是I—-6e-+6OH-=IO +3H2O,右侧发生反应:2H++2e-=H2↑所以发生反应的总化学方程式:KI+3H2O
+3H2O,右侧发生反应:2H++2e-=H2↑所以发生反应的总化学方程式:KI+3H2O KIO3+3H2↑,正确;D.如果用阳离子交换膜代替阴离子交换膜,阳极电极反应是:2I—-2e-=I2,阴极电极反应是:2H2O+2e-=H2↑+2OH-,所以电解槽内发生的总化学反应会发生变化,错误。
KIO3+3H2↑,正确;D.如果用阳离子交换膜代替阴离子交换膜,阳极电极反应是:2I—-2e-=I2,阴极电极反应是:2H2O+2e-=H2↑+2OH-,所以电解槽内发生的总化学反应会发生变化,错误。
考点:考查电化学反应原理,主要是电极反应式的书写及电极的判断的知识。

练习册系列答案
相关题目


 [Fe(SCN) ]2+ 。
[Fe(SCN) ]2+ 。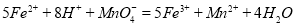 。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
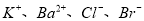
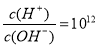 的溶液中:
的溶液中: